
Wetenschap
Wat is calciumchloride en watervergelijking?
De reactie tussen calciumchloride (CaCl₂) en water (H₂o) is een oplossingsreactie , wat betekent dat het calciumchloride oplost in het water.
Hier is de chemische vergelijking:
cacl₂ (s) + h₂o (l) → ca²⁺ (aq) + 2cl⁻ (aq)
Verklaring:
* cacl₂ (s) :Vast calciumchloride
* h₂o (l) :Vloeibaar water
* ca²⁺ (aq) :Calciumionen opgelost in water (waterig)
* 2cl⁻ (aq) :Chloride -ionen opgelost in water (waterig)
Sleutelpunten:
* Deze reactie is exotherme , wat betekent dat het warmte vrijgeeft. U zult merken dat de oplossing warmer wordt.
* Calciumchloride is een zeer oplosbaar zout in water.
* Deze reactie vormt een elektrolytoplossing , wat betekent dat het elektriciteit leidt vanwege de opgeloste ionen.
Laat het me weten als je nog andere vragen hebt!
 Apothekers stellen manieren voor om de activiteit van levofloxacine te verhogen en bacteriële resistentie te overwinnen
Apothekers stellen manieren voor om de activiteit van levofloxacine te verhogen en bacteriële resistentie te overwinnen  Is chloorgas vloeibaar bij -35 graden Celsius onder normale druk een chemische of fysische verandering?
Is chloorgas vloeibaar bij -35 graden Celsius onder normale druk een chemische of fysische verandering?  Wat is het molecuulgewicht van koolstof?
Wat is het molecuulgewicht van koolstof?  Defecten in nanodeeltjes helpen de productie van waterstof te stimuleren, een schoon brandende brandstof
Defecten in nanodeeltjes helpen de productie van waterstof te stimuleren, een schoon brandende brandstof Niet-giftige technologie haalt meer goud uit erts
Niet-giftige technologie haalt meer goud uit erts
 Welke soorten weersomstandigheden doet Texas?
Welke soorten weersomstandigheden doet Texas?  Beschrijf 2 voorwaarden op aarde die de planeet gunstig maken voor het leven?
Beschrijf 2 voorwaarden op aarde die de planeet gunstig maken voor het leven?  Bahamas, Florida zet zich schrap als nieuwe orkaan Isaias neerstort
Bahamas, Florida zet zich schrap als nieuwe orkaan Isaias neerstort Nieuwe brand ontsteekt in de buurt van LA terwijl felle bosbranden in Californië woeden
Nieuwe brand ontsteekt in de buurt van LA terwijl felle bosbranden in Californië woeden Hoe kan territoriaal ecologisch herstel van provincies worden gebruikt om de koolstofputten te vergroten?
Hoe kan territoriaal ecologisch herstel van provincies worden gebruikt om de koolstofputten te vergroten?
Hoofdlijnen
- Wat is de formule voor suiker?
- Wat betekent anibus in de wetenschap?
- Wat betekent zeggen dat een cel ontplooiing is?
- Begrazing met lage intensiteit is lokaal beter voor de biodiversiteit, maar uitdagend voor landgebruikers, blijkt uit onderzoek
- Plagen van wespen? Een wetenschapper legt uit waarom je niet in paniek moet raken over geruchten over een groeiende bevolking
- Vat de observaties en gevolgtrekkingen erkend als ruggengraat van evolutie samen door natuurlijke selectie?
- Bewaken van genetische mutaties die belangrijk zijn voor panterbeheer in Florida
- Wat is fotosytem I en II?
- Hoe regelt de celmembraanbeweging van materialen in en uit cel?
- Een methode om afgebroken perovskiet in zonnecellen te vervangen door ze recyclebaar te maken

- Nieuw gesynthetiseerde AM-III-koolstof is tot nu toe het hardste en sterkste amorfe materiaal

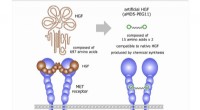
- Wetenschappers verkrijgen met succes een synthetische groeifactor die compatibel is met het inheemse eiwit
- Verbeterde afvalscheiding door superstabiele magnetische vloeistof

- Neutronendiffractie-experimenten van materialen met structuren die meerdere metalen elementen bevatten

 Wat betekent niet -naald?
Wat betekent niet -naald?  Bereken de zwaartekracht op een massa van 1 kg op het aardoppervlak De aarde is 6 x 1024 en straal 6,4 10 6m?
Bereken de zwaartekracht op een massa van 1 kg op het aardoppervlak De aarde is 6 x 1024 en straal 6,4 10 6m?  Beschrijf het gedrag van golven wanneer ze een oppervlak slaan?
Beschrijf het gedrag van golven wanneer ze een oppervlak slaan?  Waarom voegen boeren kalksteen toe aan de bodem?
Waarom voegen boeren kalksteen toe aan de bodem?  Is stenen berg constructief en destructief landvorm?
Is stenen berg constructief en destructief landvorm?  Wat is de wetenschappelijke naam of taxonomische classificatie van Giftous Plant Gemmed Amanita?
Wat is de wetenschappelijke naam of taxonomische classificatie van Giftous Plant Gemmed Amanita?  Wetenschapsvaartuig voor oceaanmissie arriveert in Seychellen
Wetenschapsvaartuig voor oceaanmissie arriveert in Seychellen Welke groep planten domineert de aarde?
Welke groep planten domineert de aarde?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

