
Wetenschap
Wat zijn voorbeelden van amfoterische oxiden?
voorbeelden van amfoterische oxiden:
Amfoterische oxiden zijn chemische verbindingen die kunnen werken als zowel zuren als basen, afhankelijk van de chemische omgeving. Hier zijn enkele voorbeelden:
Gemeenschappelijke voorbeelden:
* aluminiumoxide (al₂o₃): Reageert met zuren om zouten en water te vormen, en met basen om aluminaten te vormen.
* zinkoxide (ZnO): Reageert met zuren om zinkzouten en water te vormen, en met basen om zinkaten te vormen.
* lood (ii) oxide (PBO): Reageert met zuren om loodzouten en water te vormen, en met basen om siten te vormen.
* tin (ii) oxide (sno): Reageert met zuren om blikzouten en water te vormen, en met basen om stannieten te vormen.
* chroom (iii) oxide (cr₂o₃): Reageert met zuren om chroomzouten en water te vormen, en met basen om chromieten te vormen.
Minder veel voorkomende voorbeelden:
* berylliumoxide (beo)
* galliumoxide (Ga₂o₃)
* indiumoxide (in₂o₃)
* germaniumdioxide (geo₂) (soms geclassificeerd als zuur)
Opmerking:
* De classificatie van een oxide als amfoterisch kan afhangen van de specifieke omstandigheden, zoals temperatuur en concentratie.
* Sommige oxiden, zoals sio₂ (siliciumdioxide) en p₄o₁₀ (fosfor pentoxide) , worden meestal als zuur beschouwd, maar kan onder bepaalde omstandigheden amfoterisch gedrag vertonen.
reacties die amfoterisch gedrag aantonen:
aluminiumoxide als zuur:
Al₂o₃ + 6Hcl → 2alcl₃ + 3h₂o
aluminiumoxide als basis:
Al₂o₃ + 2naOH + 3H₂O → 2NA [AL (OH) ₄]
zinkoxide als zuur:
ZnO + 2HCl → ZnCl₂ + H₂o
zinkoxide als basis:
ZnO + 2naOH + H₂o → Na₂ [Zn (OH) ₄]
Deze voorbeelden laten zien dat amfoterische oxiden kunnen reageren met zowel zuren als basen om zouten en water te vormen. Deze unieke eigenschap maakt ze waardevol in verschillende toepassingen, waaronder productie, katalyse en pigmenten.
 Luchtfoto's van planthoogten kunnen boeren helpen om veldgewassen effectiever te beheren
Luchtfoto's van planthoogten kunnen boeren helpen om veldgewassen effectiever te beheren Voorspellers kijken misschien op de verkeerde plaats bij het voorspellen van tornado's, uit onderzoek blijkt
Voorspellers kijken misschien op de verkeerde plaats bij het voorspellen van tornado's, uit onderzoek blijkt Wat zijn dingen die we doen die de aarde pijn doen?
Wat zijn dingen die we doen die de aarde pijn doen?  Wat is Ra de god?
Wat is Ra de god?  Ruimte is de sleutel tot monitoring van de verzuring van de oceaan
Ruimte is de sleutel tot monitoring van de verzuring van de oceaan
Hoofdlijnen
- Prokaryotische versus eukaryotische cellen:wat is het verschil?
- Welk concept van evolutie is gebaseerd op De Lamarck?
- Wat zijn de functies van het irisdiafragma op een microscoop?
- Hoe zijn allelesfrequenties gerelateerd aan genenpools?
- Welke omstandigheden kunnen de groei van bacteriën hebben bevorderd?
- Is een plantencel dood of levend?
- Trechtervisie:nieuwe informatie over hoe cellen in het oog helpen licht naar het netvlies te geleiden
- Wat zijn twee redenen waarom aquatische algen belangrijk zijn?
- Wat is het kenmerk van een celmembraan dat regelt welke stoffen cel kunnen binnenkomen en verlaten?
- Het maken van middeleeuwse bling

- Waarom toekomstige huizen gemaakt kunnen worden van levende schimmel

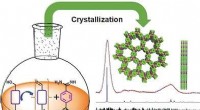
- Superieure fotokatalysatoren - covalent, kristallijne triazine-frameworks
- Hiërarchisch 3D-printen van nanoporeus goud kan een revolutie teweegbrengen in het ontwerp van elektrochemische reactoren

- Video:De chemie achter verschillende theesmaken

 Welke cellen fagocytiseren een antigeen?
Welke cellen fagocytiseren een antigeen?  Het begrijpen van secundaire lichtemissie door plasmonische nanostructuren kan medische beeldvorming verbeteren
Het begrijpen van secundaire lichtemissie door plasmonische nanostructuren kan medische beeldvorming verbeteren Hoe beïnvloeden zwaartekracht en wrijving de rotsen van de rotsen op een berghelling?
Hoe beïnvloeden zwaartekracht en wrijving de rotsen van de rotsen op een berghelling?  3D virtueel snijden van een antieke viool onthult oude lakmethoden
3D virtueel snijden van een antieke viool onthult oude lakmethoden Kosmische dageraad vond plaats 250 tot 350 miljoen jaar na de oerknal
Kosmische dageraad vond plaats 250 tot 350 miljoen jaar na de oerknal Welke botten produceren beenmerg?
Welke botten produceren beenmerg?  Porsche eerste Duitse autofabrikant die dieselmotoren verlaat
Porsche eerste Duitse autofabrikant die dieselmotoren verlaat Hoe roestvrij staal Magnetic
Hoe roestvrij staal Magnetic
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

