
Wetenschap
Wat is de relatieve massasormule van waterstofgas?
De relatieve massaformule voor waterstofgas (H₂) is eenvoudig:
2
Dit is waarom:
* Atomaire massa van waterstof: Waterstof (H) heeft een atoommassa van ongeveer 1 atomaire massa -eenheid (AMU).
* Diatomic molecuul: Waterstofgas bestaat als een diatomisch molecuul, wat betekent dat twee waterstofatomen aan elkaar binden (H₂).
* Relatieve massaberekening: Omdat elk waterstofatoom een relatieve massa van 1 heeft, is de relatieve massa van twee waterstofatomen (H₂) 1 + 1 =2.
Daarom is de relatieve massaformule van waterstofgas 2 .
 Onderzoek toont illegale hoeveelheden arseen aan in babyvoeding
Onderzoek toont illegale hoeveelheden arseen aan in babyvoeding De kust doseren:de lekkende leidingen van Baltimore County genezen de Chesapeake Bay
De kust doseren:de lekkende leidingen van Baltimore County genezen de Chesapeake Bay Welke rol speelt de mens in een ecosysteem?
Welke rol speelt de mens in een ecosysteem?  Indiase rechtbank dringt aan op nationale noodverklaring wegens hittegolven
Indiase rechtbank dringt aan op nationale noodverklaring wegens hittegolven  De aquifer van de hoogvlakten:kunnen we het volhouden?
De aquifer van de hoogvlakten:kunnen we het volhouden?
Hoofdlijnen
- Welk organisme vermenigvuldigt zich snel op basis van zijn wijze van aseksuele reproductie?
- Wetenschappers ontcijferen hoe planten zonnebrand voorkomen
- Kunnen stikstof direct worden gebruikt door levende wezens?
- Naar welke voedselchemicaliën behoort glycogeen?
- Nieuw inzicht in unieke plantchemicaliën kan toekomstige medicijnontwikkeling informeren
- Het symposium in Pittsburgh antwoordt:Wat is Watson?
- Wat is de juiste uitspraak over bryofyten? A hebben gespecialiseerde weefsels die water geleiden. B. Opgenomen door osmose. C. Zijn niet erg afhankelijk van de D-plantengroep bestaande uit algen en mossen.
- Wat is de rol van glucose in het lichaam?
- Geef de haaien niet de schuld:uit onderzoek blijkt waarom er steeds meer gehaakte tarpoenen worden gegeten
- Efficiënte opname van uranium(VI) gerealiseerd door gelaagd mangaanthiofosfiet geïntercaleerd met ammonium

- Biologisch geïnspireerde kunstmatige spieren gemaakt van motoreiwitten
- Windturbinebladen kunnen ooit worden gerecycled tot zoete lekkernijen

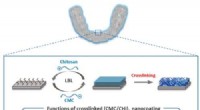
- Tandhouders en aligners helpen om bacteriën te bestrijden
- Chemische binding versus elektromagnetische golven

 Wanneer wordt de kern zichtbaar in mitose?
Wanneer wordt de kern zichtbaar in mitose?  Over spanningsverminderingsweerstand Formula
Over spanningsverminderingsweerstand Formula VN warm op het spoor van temperatuurrecords
VN warm op het spoor van temperatuurrecords Wanneer aminozuren worden gedeamineerd, welke bron kunnen ze worden gebruikt?
Wanneer aminozuren worden gedeamineerd, welke bron kunnen ze worden gebruikt?  Is Cynobacteria het eerste levende organisme op aarde?
Is Cynobacteria het eerste levende organisme op aarde?  Waar valt een neutronenster op het Hertzsprung-Russell-diagram in relatie tot andere stellaire objecten?
Waar valt een neutronenster op het Hertzsprung-Russell-diagram in relatie tot andere stellaire objecten?  Hoe evoluerende landschappen de vroege migratiepatronen van First Peoples naar Australië beïnvloedden
Hoe evoluerende landschappen de vroege migratiepatronen van First Peoples naar Australië beïnvloedden  Grafenen die licht laten schijnen, kunnen leiden tot supersnel internet
Grafenen die licht laten schijnen, kunnen leiden tot supersnel internet
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

