
Wetenschap
Hoe zijn een zwavelmolecuul en dioxide vergelijkbaar?
* zwavel (s):
* Bestaat als een vaste stof bij kamertemperatuur.
* Bestaat uit acht zwavelatomen die samen in een ring zijn verbonden (S8).
* Heeft geen zuurstof.
* Is een gele, brosse vaste stof.
* zwaveldioxide (SO2):
* Bestaat als een gas bij kamertemperatuur.
* Bestaat uit één zwavelatoom gebonden aan twee zuurstofatomen.
* Heeft zuurstof.
* Is een kleurloos gas met een scherpe geur.
overeenkomsten:
* Beide bevatten zwavel.
* Beide zijn belangrijk in industriële processen en milieuproblemen.
Belangrijkste verschillen:
* Chemische samenstelling: Zwavel is een puur element, terwijl zwaveldioxide een verbinding is.
* Fysieke toestand: Zwavel is een vaste, zwaveldioxide is een gas.
* geur: Zwavel is reukloos, zwaveldioxide heeft een scherpe geur.
* toxiciteit: Zwavel is relatief niet-toxisch, zwaveldioxide is een giftig gas.
Het is belangrijk om te begrijpen dat zwavel- en zwaveldioxide zeer verschillende stoffen zijn met verschillende eigenschappen.
 Welke atomen van de halogeenfamilie -elementen krijgen meestal twee elektronen als ze reageren?
Welke atomen van de halogeenfamilie -elementen krijgen meestal twee elektronen als ze reageren?  Waarom wordt het natriumbenzoaat gemakkelijk geëxtraheerd in H20, terwijl het oorspronkelijke benzoëzuur geen H20 is?
Waarom wordt het natriumbenzoaat gemakkelijk geëxtraheerd in H20, terwijl het oorspronkelijke benzoëzuur geen H20 is?  Is uw drinkwater veilig?
Is uw drinkwater veilig?  Wat gebeurt er met de deeltjes van een vloeistof als deze bevriest?
Wat gebeurt er met de deeltjes van een vloeistof als deze bevriest?  Waarom vormen elementen ionische en/of covalente bindingen?
Waarom vormen elementen ionische en/of covalente bindingen?
 Stof uit de Sahara verstikt Zwitserland en Zuidoost-Frankrijk
Stof uit de Sahara verstikt Zwitserland en Zuidoost-Frankrijk  Android-telefoons om aardbevingen te volgen; Californië krijgt waarschuwingssysteem
Android-telefoons om aardbevingen te volgen; Californië krijgt waarschuwingssysteem Hoe komt water de atmosfeer van de aarde binnen?
Hoe komt water de atmosfeer van de aarde binnen?  Hoe we de effectiviteit van wereldwijde milieubescherming kunnen vergroten
Hoe we de effectiviteit van wereldwijde milieubescherming kunnen vergroten Welke discipline heeft bewijs gevonden voor evolutie op basis van de inheemse verdelingen van levende soorten?
Welke discipline heeft bewijs gevonden voor evolutie op basis van de inheemse verdelingen van levende soorten?
Hoofdlijnen
- Onderzoek onderzoekt waarom mensen eerder van etniciteit veranderen
- Hoe doodt alcohol bacteriën?
- Waarom krullen wortels? Onderzoek onthult de mechanismen achter de veroudering van wortelgroenten
- Wat zijn de vier macromoleculen van het leven?
- Wat zou een homologe structuur zijn voor menselijke armbeen?
- Hoe voorzien eencellige organismen in hun basisbehoeften?
- Wat is de betekenis van gemeenschappelijk laboratoriumapparatuur in de wetenschap?
- Wie heeft mannen nodig? Vrouwelijke haaien maken alleen baby's in Italië
- Welke fase van mitose scheiden de gerepliceerde chromosomen?
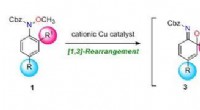
- Efficiënte synthese van meervoudig gesubstitueerde anilinen door domino-omlegging
- Smeltglazen van niet-smeltbare verbindingen
- Milieuvriendelijke productie van amandelzuur
- De vorm van zachte materie veranderen met behulp van logische circuits gemaakt van DNA
- Neutronen en röntgenstralen gebruiken om de veroudering van lithiumbatterijen te analyseren

 Wat is de datum dat op aarde gecentreerd zonnestelsel werd beschouwd als een zonnestelsel?
Wat is de datum dat op aarde gecentreerd zonnestelsel werd beschouwd als een zonnestelsel?  Waarom hebben vulkanen gletsjers op hun hellingen?
Waarom hebben vulkanen gletsjers op hun hellingen?  Kippenplastic en wijnleer – afval een nieuw leven geven
Kippenplastic en wijnleer – afval een nieuw leven geven Wat is de term die wordt gebruikt om fysieke en culturele kenmerken van de aarde te beschrijven?
Wat is de term die wordt gebruikt om fysieke en culturele kenmerken van de aarde te beschrijven?  Hoeveel kilo is 7lb?
Hoeveel kilo is 7lb?  Zijn cellen gemaakt van iets kleiner?
Zijn cellen gemaakt van iets kleiner?  Algebra 1 in vergelijking met Algebra 2
Algebra 1 in vergelijking met Algebra 2 Meer mensen betekent altijd minder Afrikaanse carnivoren, toch? Nee
Meer mensen betekent altijd minder Afrikaanse carnivoren, toch? Nee
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

