
Wetenschap
Waarom vormt zwaveldioxide een zure oplossing?
1. Oplost in water: Wanneer zwaveldioxidegas oplost in water, reageert het met de watermoleculen.
2. Vorming van zwavelzuur: De reactie vormt zwavelzuur (h₂so₃):
So₂ (G) + H₂o (L) ⇌ H₂so₃ (aq)
3. Zure eigenschappen van zwavelzuur: Zwavelzuur is een zwak zuur, wat betekent dat het gedeeltelijk ioniseert in water, waardoor waterstofionen (H⁺) en bisulfietionen (HSO₃⁻) worden vrijgeeft:
H₂so₃ (aq) ⇌ H⁺ (aq) + hso₃⁻ (aq)
4. Verhoogde waterstofionconcentratie: De aanwezigheid van waterstofionen in de oplossing maakt het zuur.
Samenvattend: Zwaveldioxide reageert met water om zwavelzuur te vormen, dat vervolgens waterstofionen vrijgeeft, waardoor de oplossing zuur wordt.
 Geuren langer laten duren
Geuren langer laten duren Wat zijn twee gebruik van zuurstof?
Wat zijn twee gebruik van zuurstof?  Teamwetenschap leidt tot doorbraak in kooldioxideomzetting
Teamwetenschap leidt tot doorbraak in kooldioxideomzetting Wat is 1 het kleinste deel van een compound die nog steeds de eigenschappenverbinding heeft?
Wat is 1 het kleinste deel van een compound die nog steeds de eigenschappenverbinding heeft?  Een eenstaps multikatalytische methode om racemische mengsels te verrijken tot een enkele enantiomeer
Een eenstaps multikatalytische methode om racemische mengsels te verrijken tot een enkele enantiomeer
 Een floristische vereniging gedomineerd door hoge grassen en gevonden op de middelste breedtegraden is?
Een floristische vereniging gedomineerd door hoge grassen en gevonden op de middelste breedtegraden is?  Behoud en naamloze regenwormen:beoordelaars in het duister?
Behoud en naamloze regenwormen:beoordelaars in het duister?  Klimaatbereide landen verliezen terrein, recente indexshows
Klimaatbereide landen verliezen terrein, recente indexshows Wat nemen planten uit hun omgeving?
Wat nemen planten uit hun omgeving?  NASA-satelliet kijkt naar tropische storm Kikos wolkenhoogten, temperaturen
NASA-satelliet kijkt naar tropische storm Kikos wolkenhoogten, temperaturen
Hoofdlijnen
- Zijn cellen gemaakt van iets kleiner?
- Welk deel van een walvis wordt Balleen genoemd?
- Wat is de wetenschappelijke classificatie van spinazie?
- Inzicht in de manier waarop bruinrotschimmels hout afbreken, zou kunnen leiden tot nieuwe hulpmiddelen voor een efficiëntere productie van biobrandstoffen
- Brengt de moderne synthese van evolutie het bewijsmateriaal voor en ideeëngenetica samen?
- Hoe komt bacteriën mensen ten goede?
- Wat is de naam van nucleotiden heeft geen DNA en RNA?
- Genetische ontdekking kan leiden tot betere behandelingen voor veelvoorkomende tumoren bij honden
- Wat zijn cellen in het kraakbeen gestimuleerd om te worden?
- Natuurkundige maakt ademhalingstoestellen van het type N95 met een suikerspinmachine

- Deze microben eten elektronen voor energie
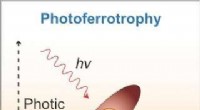
- Onderzoekers stellen een eenstapsstrategie voor om op grafeen gebaseerde composietfaseveranderingsmaterialen te synthetiseren
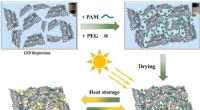
- Stam gebruiken om oxynitride-eigenschappen te beheersen

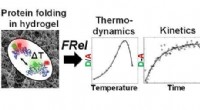
- Onderzoek naar vouwstabiliteit en dynamiek van eiwitten
 Welke laag van de zon beweegt warmte van stralend naar fotosfeer?
Welke laag van de zon beweegt warmte van stralend naar fotosfeer?  Waarom lijken de sterren 360 graden te verplaatsen in 24 uur?
Waarom lijken de sterren 360 graden te verplaatsen in 24 uur?  Manieren om windenergie te besparen
Manieren om windenergie te besparen Waarom is het moeilijk om laseractie te bereiken bij een hoger frequentiebereik?
Waarom is het moeilijk om laseractie te bereiken bij een hoger frequentiebereik?  Is hydroxide een element of een verbinding?
Is hydroxide een element of een verbinding?  Zijn kometen meestal gemaakt van rock en metal?
Zijn kometen meestal gemaakt van rock en metal?  Wat is het proces waarmee voedingsmoleculen worden verplaatst naar de bloedbaan die wordt genoemd?
Wat is het proces waarmee voedingsmoleculen worden verplaatst naar de bloedbaan die wordt genoemd?  Wat was de bijdrage van Hans en Zacharias aan de wetenschap?
Wat was de bijdrage van Hans en Zacharias aan de wetenschap?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

