
Wetenschap
Waterstofbinding vindt plaats in moleculen waar waterstof is gebonden aan welke elementen fluor koolstofzuurstof stikstofboor?
Dit is waarom:
* Hoge elektronegativiteit: Deze drie elementen hebben een hoge elektronegativiteit, wat betekent dat ze elektronen sterk aantrekken. Wanneer gebonden aan waterstof, besteden de gedeelde elektronen meer tijd rond de fluor, zuurstof of stikstofatoom, waardoor een gedeeltelijke negatieve lading (δ-) op dat atoom en een gedeeltelijke positieve lading (δ+) op het waterstofatoom ontstaat.
* Strong dipoolmoment: Deze ongelijke delen van elektronen creëert een sterk dipoolmoment, met het positieve uiteinde van de dipool op het waterstofatoom en het negatieve uiteinde van het fluor-, zuurstof- of stikstofatoom.
* Vorming van waterstofbruggen: Het positieve waterstofatoom in één molecuul kan vervolgens een sterke elektrostatische aantrekkingskracht (waterstofbinding) vormen met het negatieve zuurstof, fluor of stikstofatoom van een ander molecuul.
boron neemt niet deel aan waterstofbinding. Hoewel het minder elektronegatief is dan de andere vermelde elementen, vormt het niet sterk genoeg dipolen om de nodige interacties voor waterstofbinding te creëren.
 Hoe teken je monomeren van een nuleïnezuur?
Hoe teken je monomeren van een nuleïnezuur?  Wat is carbonaatbuffering?
Wat is carbonaatbuffering?
Veel van de meest herkenbare delen van de natuur functioneren door een of andere balans te handhaven. Het carbonaatbuffersysteem is een van de belangrijkste buffersystemen in de natuur, wat helpt om dat evenwicht te handh
 Wat is de juiste formule voor verbinding gemaakt wanneer waterige oplossingen die een opgelost magnesium bevatten en chloride worden gemengd?
Wat is de juiste formule voor verbinding gemaakt wanneer waterige oplossingen die een opgelost magnesium bevatten en chloride worden gemengd?  Wat is de moderne elektronenconfiguratie van zwavel?
Wat is de moderne elektronenconfiguratie van zwavel?  Hoe werkt fotolyse?
Hoe werkt fotolyse?
Hoofdlijnen
- Nieuw onderzoek laat zien hoe dicamba veilig kan worden gebruikt in suikermaïs
- Wat is de wetenschapsdefinitie om te isoleren?
- Wat is het LRAGE -ogran in uw lichaam?
- Wat is de rol van glucose in cellulaire ademhaling?
- Wat is een voorbeeld van vooruitgang in DNA -technologie die de menselijke gezondheid rechtstreeks heeft beïnvloed?
- Wat worden granulocyten?
- Wereldwijde visbestanden kunnen niet worden hersteld als er niets wordt gedaan om klimaatverandering en overbevissing een halt toe te roepen, suggereert nieuw onderzoek
- Wat zijn enkele moleculen die bewegen door diffusie en osmose?
- Wat is fertillostion?
- Nieuwe fotogevoelige hydrogels ontwikkeld met oog voor biomedische toepassingen

- Milieuvriendelijke elektrochemische katalysatoren die zonnecellen gebruiken om energie uit de zon te halen
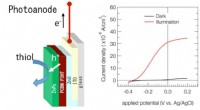
- Octopus-geïnspireerde zelfklevende patch werkt onder water

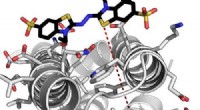
- Kunstmatige enzymfuncties evenals natuurlijke versie
- Nieuwe techniek kan een revolutie teweegbrengen in de nauwkeurigheid en detectie van biomechanische veranderingen van cellen
 Levende wezens spelen geen rol bij fysische of chemische verwering?
Levende wezens spelen geen rol bij fysische of chemische verwering?  Hoe astronomen de grootte van het zonnestelsel berekenen
Hoe astronomen de grootte van het zonnestelsel berekenen  Is de maan een lichtbron?
Is de maan een lichtbron?  Een prothese die het gevoel herstelt van waar uw hand is
Een prothese die het gevoel herstelt van waar uw hand is Extreme ultraviolette beeldvorming toont potentieel om onderzoek naar de ziekte van Alzheimer te verbeteren
Extreme ultraviolette beeldvorming toont potentieel om onderzoek naar de ziekte van Alzheimer te verbeteren Hoe u elk getal kunt wijzigen in een percentage, met Voorbeelden
Hoe u elk getal kunt wijzigen in een percentage, met Voorbeelden Hoe maak je je eigen agar voor petrischalen
Hoe maak je je eigen agar voor petrischalen Kunststofproducten kunnen gemakkelijk elektronisch worden met de eerste vormbare circuits van volledig koolstof
Kunststofproducten kunnen gemakkelijk elektronisch worden met de eerste vormbare circuits van volledig koolstof
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

