
Wetenschap
Wat is meer reactieve fluor of stikstof?
* elektronegativiteit: Fluor is het meest elektronegatieve element op het periodiek systeem. Dit betekent dat het een sterke aantrekkingskracht heeft op elektronen.
* Elektronenconfiguratie: Fluor heeft slechts nog een elektron nodig om zijn buitenste schaal te voltooien, waardoor het zeer reactief is om stabiliteit te bereiken. Stikstof heeft drie elektronen in zijn buitenste schaal, waardoor het minder enthousiast is om elektronen te krijgen.
* bindingssterkte: De bindingen gevormd door fluor zijn over het algemeen zwakker dan die gevormd door stikstof. Dit maakt het gemakkelijker om fluorbindingen te verbreken en deel te nemen aan reacties.
Samenvattend: Fluor's hoge elektronegativiteit, het verlangen om één elektron te winnen en zwakkere bindingen maken het een veel reactief element dan stikstof.
 Afbeelding:Rookwolken van branden in Turkije
Afbeelding:Rookwolken van branden in Turkije Is de aardlaag van de astenosfeer buigzaam als laffy taffy?
Is de aardlaag van de astenosfeer buigzaam als laffy taffy?  De hernieuwbare in plaats van de Roaring Twenties:een duurzaamheidsdecennium
De hernieuwbare in plaats van de Roaring Twenties:een duurzaamheidsdecennium Uit onderzoek blijkt dat ijsplaten breken onder het gewicht van smeltwatermeren
Uit onderzoek blijkt dat ijsplaten breken onder het gewicht van smeltwatermeren  Hoe zijn insecten aangepast aan het leven op het land?
Hoe zijn insecten aangepast aan het leven op het land?
Hoofdlijnen
- Van welk systeem is de schedel onderdeel?
- De twee belangrijkste manieren waarop neuronen in staat zijn om stimuli te reageren?
- Wat zijn plantenvoortplanting?
- Phototroph (Prokaryote Metabolism): Wat is het?
- Welk type variabelen zijn er in het experiment?
- Een bepaalde plantensoort wordt bestoven door een bepaalde insectensoort. De insct ed ispenden op het voor voedsel. Welke term beschrijft hoe deze relatie zich vormt?
- Hoe grotbiologie werkt
- De genetische structuur die u van uw ouders hebt geërfd, wordt uw?
- Vraag en antwoord:De dood van Noordse walvissen leidt tot gesprekken over ecologie en maritieme veiligheid
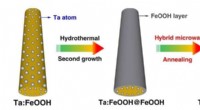
- Een stap dichter bij praktische zonne-waterstofproductie via uitgebreid gemodificeerde hematiet-fotoanode
- Kleine polymeerveren geven een boost aan het opruimen van het milieu
- Chemisch ingenieur ontwikkelt styreenvrije bio-hernieuwbare harsen

- Een betere manier om acryl te maken

- SmartFarm-apparaat oogst luchtvochtigheid voor autonoom, zelfvoorzienende stadslandbouw

 Een voorwerp valt vanuit rust op een hoogte van 128 m. Zoek de afstand die hij aflegt tijdens zijn laatste seconde in de lucht.?
Een voorwerp valt vanuit rust op een hoogte van 128 m. Zoek de afstand die hij aflegt tijdens zijn laatste seconde in de lucht.?  Wat is de relatie tussen chemie en biologie?
Wat is de relatie tussen chemie en biologie?  Cyberaanvallen een groot probleem voor alle bedrijfsgroottes, economische onzekerheid een goede tweede, blijkt uit nieuwe enquête
Cyberaanvallen een groot probleem voor alle bedrijfsgroottes, economische onzekerheid een goede tweede, blijkt uit nieuwe enquête Hoe registreren en interpreteren wetenschapper gegevens?
Hoe registreren en interpreteren wetenschapper gegevens?  Wat is de meest breedste categorie voor specifiek in DNA van genetisch materiaal?
Wat is de meest breedste categorie voor specifiek in DNA van genetisch materiaal?  2,45 cm gelijk aan hoeveel inches?
2,45 cm gelijk aan hoeveel inches?  Komt het noorderlicht een keer per jaar?
Komt het noorderlicht een keer per jaar?  RPM versus Angular Velocity
RPM versus Angular Velocity
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

