
Wetenschap
Chloorgas wordt door een calciumbromide -oplossing gebobbeld Welk type reactie is gemaakt?
* chloor (Cl₂) is meer reactief dan broom (br₂) Dit betekent dat chloor een sterkere neiging heeft om elektronen te winnen.
* De reactie: Wanneer chloorgas door een calciumbromide -oplossing wordt geborreld, verplaatsen de chlooratomen de broomionen uit de oplossing.
Hier is de evenwichtige chemische vergelijking:
Cl₂ (G) + Cabr₂ (aq) → Cacl₂ (aq) + br₂ (l)
Verklaring:
* Chloor (CL₂) reageert met calciumbromide (Cabr₂) om calciumchloride (CaCl₂) en broom te produceren (Br₂).
* De chlooratomen verplaatsen de broomionen uit de calciumbromide -oplossing, wat resulteert in de vorming van calciumchloride en vloeibare broom.
Belangrijke kenmerken van een enkele verplaatsingsreactie:
* Eén element reageert met een verbinding.
* Het meer reactieve element verplaatst een minder reactief element van de verbinding.
* De producten zijn een nieuwe verbinding en een enkel element.
 Welke 2 dingen kunnen chemische en fysieke verandering doormaken?
Welke 2 dingen kunnen chemische en fysieke verandering doormaken?  In een oplossing wordt de blanco opgelost door blanco?
In een oplossing wordt de blanco opgelost door blanco?  Waarom worden 18 groepselementen genaamd Noble Gases genaamd?
Waarom worden 18 groepselementen genaamd Noble Gases genaamd?  Nieuwe niet-covalente binding blokkeert de afstotende geur van isocyaniden
Nieuwe niet-covalente binding blokkeert de afstotende geur van isocyaniden Hoe los je een verzadigde oplossing op zonder water toe te voegen?
Hoe los je een verzadigde oplossing op zonder water toe te voegen?
 Ontbindende bladeren zijn een verrassende bron van broeikasgassen
Ontbindende bladeren zijn een verrassende bron van broeikasgassen Zware stikstofmoleculen onthullen touwtrekken op planetaire schaal
Zware stikstofmoleculen onthullen touwtrekken op planetaire schaal Nieuw lab op een chip kan inspanningen voor koolstofopslag versnellen
Nieuw lab op een chip kan inspanningen voor koolstofopslag versnellen Hoe lieten dinosaurussen sporen achter in massieve steen?
Hoe lieten dinosaurussen sporen achter in massieve steen?  Grote hoeveelheden waardevolle energie, voedingsstoffen, water verloren in snel stijgende afvalwaterstromen ter wereld
Grote hoeveelheden waardevolle energie, voedingsstoffen, water verloren in snel stijgende afvalwaterstromen ter wereld
Hoofdlijnen
- Wat stellen biologen een vraag over en het gebruik van het wetenschappelijke proces?
- Wat maakt dominante allelen anders dan recessieve allelen?
- Waarom bevatten cellen zowel macromoleculen als kleine koolstofverbindingen?
- Wat gebruiken cellen om stoffen te transporteren?
- Welke methode gebruiken wetenschappers om identieke nakomelingen te maken uit volwassen cellen?
- Hoe u uw hond kunt trainen in de basisvaardigheden van het leven, en waarom dit belangrijk is
- Wat zit er in een naam? In sommige gevallen een langere levensduur
- Waar krijgt een plant voedingsstoffen?
- Van schimmels tot mode:Mushroom eco-leer beweegt zich richting de mainstream
- Onderzoekers onderzoeken de structuur van fosfaationische geleidende glazen met behulp van vastestof NMR
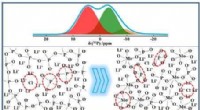
- Eiwitporiën verpakt in polymeren maken superefficiënte filtratiemembranen

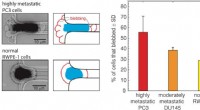
- Nieuwe techniek belooft verbeterde detectie van uitgezaaide prostaatkanker
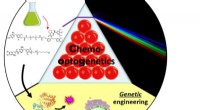
- Een potje poolen in de live cell
- Nieuwe techniek kan de productie van afval naar methaan versnellen

 Hoeveel kilometer calciumnitraat zou reageren met 4,55 mol chroom (III) sulfaat om chroomnitraat te produceren?
Hoeveel kilometer calciumnitraat zou reageren met 4,55 mol chroom (III) sulfaat om chroomnitraat te produceren?  Hoeveel mol NaOH zijn er nodig om 2 liter een 2,0 M oplossing te bereiden?
Hoeveel mol NaOH zijn er nodig om 2 liter een 2,0 M oplossing te bereiden?  Wat is de naam van het maken van mRNA Copt A Gene?
Wat is de naam van het maken van mRNA Copt A Gene?  Slim medicijnafgiftesysteem -- Gouden nanokooi bedekt met polymeer (met video)
Slim medicijnafgiftesysteem -- Gouden nanokooi bedekt met polymeer (met video) Wat voor soort kaart maakt gebruik van breedtegraad en lengtegraad?
Wat voor soort kaart maakt gebruik van breedtegraad en lengtegraad?  Nieuw thermo-elektrisch nanoantenne-ontwerp voor gebruik bij het oogsten van zonne-energie
Nieuw thermo-elektrisch nanoantenne-ontwerp voor gebruik bij het oogsten van zonne-energie Gemeenschappelijke benadering van diversiteit in het hoger onderwijs weerspiegelt de voorkeuren van blanke Amerikanen
Gemeenschappelijke benadering van diversiteit in het hoger onderwijs weerspiegelt de voorkeuren van blanke Amerikanen Hoe zijn Lunar Eclipse zowel voor Eclipsse op zonne -energie?
Hoe zijn Lunar Eclipse zowel voor Eclipsse op zonne -energie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

