
Wetenschap
Waarom accepteert een negatief chlooratoom gemakkelijk een ander elektron?
* Elektronenconfiguratie: Chloor heeft 7 elektronen in zijn buitenste schaal. Door één elektron te winnen, bereikt het een stabiele octetconfiguratie, waarbij de Octet -regel wordt vervuld. Dit maakt Cl- een negatief geladen ion.
* afstoting: Het toevoegen van een ander elektron aan CL- zou een zeer onstabiele soort creëren met twee extra elektronen in de buitenste schaal. Dit zou resulteren in een significante afstoting tussen de negatief geladen elektronen, waardoor het zeer ongunstig is.
* Elektrostatische krachten: De negatieve lading op Cl- afstoot al andere negatief geladen deeltjes. Het aantrekken van een ander elektron zou deze afstoting verder intensiveren.
Samenvattend: Cl- is al stabiel met een volledig octet en een negatieve lading. Het zou een aanzienlijke hoeveelheid energie vereisen om de elektrostatische afstoting te overwinnen en te dwingen om een ander elektron te accepteren.
 Detectie van meerdere sepsis-biomarkers uit volbloed - snel gemaakt, nauwkeurig, en goedkoop
Detectie van meerdere sepsis-biomarkers uit volbloed - snel gemaakt, nauwkeurig, en goedkoop Nauwkeurige analyse van de deeltjessamenstelling van smog
Nauwkeurige analyse van de deeltjessamenstelling van smog Smeltend en kookpunt van zilver?
Smeltend en kookpunt van zilver?  Wat is de intermoleculaire kracht die wordt aangetroffen in waterstofsulfide?
Wat is de intermoleculaire kracht die wordt aangetroffen in waterstofsulfide?  Worden ionische verbindingen gevormd door metalen?
Worden ionische verbindingen gevormd door metalen?
 NASA onderzoekt waterdampconcentratie van tropische cycloon Belnas
NASA onderzoekt waterdampconcentratie van tropische cycloon Belnas De explosie die de ionosfeer deed schudden
De explosie die de ionosfeer deed schudden Superbug-gen gevonden op een van de meest afgelegen plekken op aarde
Superbug-gen gevonden op een van de meest afgelegen plekken op aarde Welke risico's kunnen huisdierenhamsters en gerbils in Australië met zich meebrengen?
Welke risico's kunnen huisdierenhamsters en gerbils in Australië met zich meebrengen?  Wetenschappers identificeren hoe de ontleding van Arctische landschappen verandert door de steeds snellere klimaatverandering
Wetenschappers identificeren hoe de ontleding van Arctische landschappen verandert door de steeds snellere klimaatverandering
Hoofdlijnen
- Welk eiwit is dat?
- Wetenschappers ontcijferen mechanismen die ten grondslag liggen aan de biologie van veroudering
- Noem twee planten die groeien uit sporen en geen zaden?
- Wat zijn de ingangen en uitgangen van cellulaire ademhaling?
- Wat is patroonvorming?
- Is bacteriecel een prokaryotisch of eukaryotisch?
- Wat is het polymeer van DNA dat bekend staat?
- Hoe neuronale herkenning van zangvogelgeluiden zich in de loop van de tijd ontvouwt
- Onderzoek wijst uit hoe de identiteit van huidcellen kan worden gedemonteerd om stamcellen te creëren
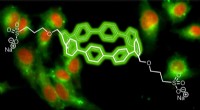
- Chemici maken circulaire fluorescerende kleurstoffen voor biologische beeldvorming
- Chemicaliënvrij, goedkope opbergzakken voor gewassen die voedsel langer bewaren nu in de handel verkrijgbaar

- Ingenieurs veranderen plastic isolator in warmtegeleider

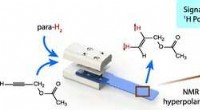
- Onderzoek naar nieuwe medicijnen kan de behoefte aan proefdieren drastisch verminderen
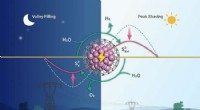
- Zeer efficiënte maliënkolderkatalysatoren ontwikkeld voor ontkoppelde waterelektrolyse
 Wat is het nucleïnezuur centraal in het metabolisme?
Wat is het nucleïnezuur centraal in het metabolisme?  Tropische cycloon Trevor vult Australische Golf van Carpentaria in NASA-afbeelding
Tropische cycloon Trevor vult Australische Golf van Carpentaria in NASA-afbeelding Wat zijn twee soorten eukaryoten met een celwand?
Wat zijn twee soorten eukaryoten met een celwand?  Sulfide en ijzer werken samen om een nieuw pad te onthullen voor de vastlegging van radionucliden
Sulfide en ijzer werken samen om een nieuw pad te onthullen voor de vastlegging van radionucliden Wat voor soort bomen worden gevonden in het boreale bos?
Wat voor soort bomen worden gevonden in het boreale bos?  Timing van regelgevende stick en ondersteunende wortel kan bedrijven gefocust houden
Timing van regelgevende stick en ondersteunende wortel kan bedrijven gefocust houden Is Mercurius vergelijkbaar met andere planeten?
Is Mercurius vergelijkbaar met andere planeten?  Nieuw ultradiffuus sterrenstelsel gevonden in de NGC 5846-groep
Nieuw ultradiffuus sterrenstelsel gevonden in de NGC 5846-groep
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

