
Wetenschap
Wat is de pH van natriumfluoride?
Dit is waarom:
* Hydrolyse: Wanneer NAF oplost in water, reageert het fluoride-ion (F-) met water om een kleine hoeveelheid hydroxide-ionen (OH-) en hydrofluorzuur (HF) te produceren:
F- + H2O ⇌ HF + OH-
* evenwicht: Deze reactie bereikt een evenwicht, wat betekent dat de snelheid van de voorwaartse en omgekeerde reacties gelijk is. De positie van dit evenwicht bepaalt de pH.
* concentratie: Een hogere concentratie van NAF zal resulteren in een hogere concentratie OH-ionen, waardoor de oplossing eenvoudiger wordt (hogere pH). Een lagere concentratie van NAF zal resulteren in een lagere concentratie OH-ionen, waardoor de oplossing minder eenvoudig is (lagere pH).
Om de pH van een specifieke NAF -oplossing te berekenen, zou u de concentratie ervan moeten weten en de evenwichtsconstante (KB) gebruiken voor de hydrolysereactie.
Belangrijke opmerking: Natriumfluoride -oplossingen zijn enigszins eenvoudig, in het algemeen met een pH tussen 7 en 8. De exacte pH kan echter variëren, afhankelijk van de concentratie.
Hoofdlijnen
- Wat biologen nog steeds niet weten over bioluminescentie
- Heeft een dierencel SAP?
- Wat zijn purines en pyrimidines?
- Experiment laat zien hoe wormgastheren en het bijbehorende microbioom gezamenlijk bijdragen aan aanpassing aan het milieu
- Wat zijn gespecialiseerde cellen en wat voor soort organisme ze hebben gevonden?
- Na de vereniging van sperma en eicel ontwikkelt de eencellige zygote zich tot een meercellig organisme met gespecialiseerde cellen door processen van?
- Grote eiwitten kunnen uit de cel worden uitgescheiden met behulp van het proces van?
- Zijn krokodillen geheime fruitliefhebbers?
- Europese zeebaars vertoont chronische verslechtering na blootstelling aan ruwe olie
- Paleofarmaceutica uit Baltisch barnsteen kunnen resistente infecties bestrijden

- Nieuwe moleculaire sondes voor opioïde receptoren

- Ontwikkeld materiaal dat tegelijkertijd warmte-isolerend en warmtegeleidend is

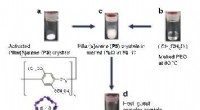
- Selectie van molecuulgewichtpolymeer door eendimensionale opsluiting
- Onderzoekers stellen vast hoe sorptiematerialen koolstof vangen en afgeven

 Luister niet naar de rijken - ongelijkheid is slecht voor iedereen
Luister niet naar de rijken - ongelijkheid is slecht voor iedereen Welk type binding zal stikstof en broomvorm vormen?
Welk type binding zal stikstof en broomvorm vormen?  Hoe creëer je energie op een woestijneiland?
Hoe creëer je energie op een woestijneiland?  Nieuwe inzichten in de belangrijkste oorzaak van een miskraam, geboorteafwijkingen ontdekt
Nieuwe inzichten in de belangrijkste oorzaak van een miskraam, geboorteafwijkingen ontdekt Waarom lijken alle sterren om de 24 uur een complete cirkel rond Polaris te maken?
Waarom lijken alle sterren om de 24 uur een complete cirkel rond Polaris te maken?  Waarom Gambia de genderquota voor vrouwen moet versnellen
Waarom Gambia de genderquota voor vrouwen moet versnellen  Auto's slecht voor kinderen en de planeet
Auto's slecht voor kinderen en de planeet Wordt cytoplasma alleen in plantencellen gevonden?
Wordt cytoplasma alleen in plantencellen gevonden?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


