
Wetenschap
Waarom lost zout of suiker niet op in kerosine?
Dit is waarom:
* polariteit: Polaire moleculen hebben een scheiding van elektrische lading, waardoor een positief en negatief einde ontstaat. Water is een geweldig voorbeeld, waarbij zijn zuurstofatoom enigszins negatief is en zijn waterstofatomen enigszins positief zijn.
* zout en suiker: Zowel zout (NaCl) als suiker (sucrose) zijn polaire moleculen. Zout is een ionische verbinding en vormt sterke elektrostatische aantrekkingskracht tussen positieve natriumionen (Na+) en negatieve chloride-ionen (Cl-). Suiker heeft een complexe structuur met veel polaire hydroxylgroepen (-OH) die ook aantrekkelijke krachten creëren.
* kerosine: Kerosine is een nonpolar koolwaterstof. Het is gemaakt van lange ketens van koolstof- en waterstofatomen, zonder significante scheiding van lading.
De regel: "Zoals oplost zoals." Dit betekent dat polaire stoffen het beste oplossen in andere polaire stoffen, en niet -polaire stoffen lossen het beste op in niet -polaire stoffen.
Waarom het niet werkt: De sterke aantrekkelijke krachten tussen het polaire zout- en suikermoleculen zijn veel sterker dan de zwakke interacties die ze kunnen vormen met niet -polaire keroseenmoleculen. Daarom kunnen ze niet uit elkaar breken en verspreiden binnen kerosine.
daarentegen: Water is een polair oplosmiddel, daarom lossen zout en suiker er gemakkelijk in op. De watermoleculen kunnen interageren met de geladen of polaire delen van zout- en suikermoleculen, waardoor ze effectief uit elkaar worden getrokken en verspreid over het water.
 Een elektron winnen om een negatief ion te vormen of?
Een elektron winnen om een negatief ion te vormen of?  Wat zijn de 6 elementen van de wetenschappelijke methode?
Wat zijn de 6 elementen van de wetenschappelijke methode?  Wat is de gemiddelde translationele kinetische energie van gasmoleculen?
Wat is de gemiddelde translationele kinetische energie van gasmoleculen?  Noordzeewater en gerecycled metaal gecombineerd om de opwarming van de aarde te helpen verminderen
Noordzeewater en gerecycled metaal gecombineerd om de opwarming van de aarde te helpen verminderen Wat is acromegly?
Wat is acromegly?
 Deep-learning algoritmen gebruiken om kaarten van scheepssporen te maken
Deep-learning algoritmen gebruiken om kaarten van scheepssporen te maken Nieuw onderzoek schetst waarom Zuid-Afrikaans-Amerikaanse boseigenaren minder snel gebruik zullen maken van federale hulp
Nieuw onderzoek schetst waarom Zuid-Afrikaans-Amerikaanse boseigenaren minder snel gebruik zullen maken van federale hulp  Hoe gletsjers aan het einde van de laatste ijstijd uit Schotland verdwenen
Hoe gletsjers aan het einde van de laatste ijstijd uit Schotland verdwenen Innovatieve overstromingskartering van onderzoekers helpt water- en noodbeheerfunctionarissen
Innovatieve overstromingskartering van onderzoekers helpt water- en noodbeheerfunctionarissen Welk type opvolging komt voor in een gebied waar het ecosysteem is verstoord?
Welk type opvolging komt voor in een gebied waar het ecosysteem is verstoord?
Hoofdlijnen
- Indringende vraag:Wat gaat er verloren als een taal sterft?
- Welke structuren worden aangetroffen in dierlijke cellen, maar niet in plantencellen?
- Wat zijn de twee hoofdcomponenten van een immuunrespons?
- Een nieuwe manier om feromonen te produceren als gewasbeschermingsmiddel
- Hoe onderzoekers naar het vogelbrein in actie kijken
- Lang of kort? Dik dun? Onderzoek toont aan dat veel factoren de arm- en beenomvang beïnvloeden
- Hoeveel sekschomosoom en autosoom bevinden zich in een menselijke somatische cel?
- Wat moet een zaad nodig hebben voor kieming?
- Een gen wiens code niet wordt uitgedrukt tenzij er een soortgelijk allel aanwezig wordt genoemd?
- Wetenschappers onthullen dynamische koppeling van sterke waterstofbrug
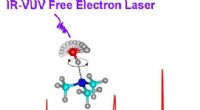
- 3D-geprinte eiwitten presteren beter dan bestaande flexibele elektronicamaterialen

- Beeldvorming van mRNA precies daar waar het is gemaakt - op de plaats van vertaling
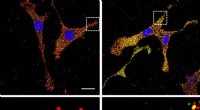
- Evolutie hacken, screeningstechniek kan het meest wijdverbreide enzym verbeteren

- Nieuwe zeolieten-zilverkatalysator verhoogt de oxidatie van formaldehyde bij lage temperaturen
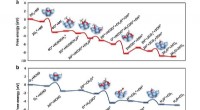
 Wat is de oorzaak van het bestaan?
Wat is de oorzaak van het bestaan?  Nanodraad-overbruggingstransistors openen de weg naar elektronica van de volgende generatie
Nanodraad-overbruggingstransistors openen de weg naar elektronica van de volgende generatie Een verandering in toonhoogte van een geluid wanneer het begint te bewegen naar of weg van je?
Een verandering in toonhoogte van een geluid wanneer het begint te bewegen naar of weg van je?  Slimme pyjama's kunnen de slaap controleren en helpen verbeteren
Slimme pyjama's kunnen de slaap controleren en helpen verbeteren Hoe kan ik stikstofgas aanmaken?
Hoe kan ik stikstofgas aanmaken?  Onder de elektronenmicroscoop -- Een 3D-beeld van een individueel eiwit
Onder de elektronenmicroscoop -- Een 3D-beeld van een individueel eiwit Subaru Telescope en New Horizons verkennen het buitenste zonnestelsel
Subaru Telescope en New Horizons verkennen het buitenste zonnestelsel Onderzoekers onderzoeken machine learning om defecten in metalen 3D-geprinte onderdelen in realtime te voorkomen
Onderzoekers onderzoeken machine learning om defecten in metalen 3D-geprinte onderdelen in realtime te voorkomen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

