
Wetenschap
Hoe kun je zien of iets organisch of anorganisch is?
Belangrijkste verschillen:
* aanwezigheid van koolstof: Organische verbindingen * Altijd* bevatten koolstof (c) atomen. Hoewel sommige anorganische verbindingen * koolstof kunnen bevatten, is het geen bepalend kenmerk.
* waterstofbinding: Organische verbindingen vormen vaak waterstofbruggen, wat leidt tot unieke eigenschappen zoals relatief hoge smelt- en kookpunten.
* Complexiteit en diversiteit: Organische moleculen zijn ongelooflijk divers, met een groot aantal mogelijke combinaties en structuren. Anorganische moleculen hebben meestal eenvoudiger structuren.
* Bio -beschikbaarheid: Organische verbindingen worden meestal geassocieerd met levende organismen. Anorganische verbindingen zijn te vinden in zowel levende als niet-levende dingen.
Voorbeelden:
organisch:
* suikers: Glucose, fructose, sucrose
* eiwitten: Enzymen, antilichamen, collageen
* vetten en oliën: Boter, plantaardige olie
* DNA en RNA: De bouwstenen van het leven
* Petroleum: Een complex mengsel van koolwaterstoffen
anorganisch:
* water (h₂o): Essentieel voor het leven maar mist koolstof.
* zout (NaCl): Een eenvoudige ionische verbinding.
* metalen: Goud (au), ijzer (fe), aluminium (al)
* Mineralen: Kwarts (Sio₂), diamant (c)
* gassen: Zuurstof (o₂), stikstof (n₂)
Belangrijke overwegingen:
* Koolstofbattende uitzonderingen: Sommige anorganische verbindingen, zoals koolstofdioxide (CO₂) en carbonaten (zoals calciumcarbonaat, caco₃), bevatten koolstof maar worden als anorganisch beschouwd vanwege hun gebrek aan complexe koolstofhydrogene bindingen.
* koolstofvrije organische stoffen: Enkele organische verbindingen, zoals ureum [(NH₂) ₂co], worden als organisch beschouwd vanwege hun structuur en binding maar missen koolstof. Deze zijn relatief zeldzaam.
Samenvattend:
De primaire manier om te zeggen of iets organisch of anorganisch is, is door te zoeken naar de aanwezigheid van koolstof, met name in de context van complexe moleculen met koolstofhydrogene bindingen.
 Hoeveel elektronen moeten worden gewonnen door atomen van CI om een edelgasregeling te vormen?
Hoeveel elektronen moeten worden gewonnen door atomen van CI om een edelgasregeling te vormen?  De waardevolle bijdrage van stress aan de thermische stabiliteit van polykristallijne legeringen met nanokorrels
De waardevolle bijdrage van stress aan de thermische stabiliteit van polykristallijne legeringen met nanokorrels Welk element heeft 6 valentie-elektronen?
Welk element heeft 6 valentie-elektronen?  Waarom wordt een waterige oplossing van natriumchloride niet gebruikt om te scheiden van chloride?
Waarom wordt een waterige oplossing van natriumchloride niet gebruikt om te scheiden van chloride?  Wat is de term voor gassen die worden uitgevoerd door aerosolen en productie die de ozonlaag vernietigen?
Wat is de term voor gassen die worden uitgevoerd door aerosolen en productie die de ozonlaag vernietigen?
 Onderzoek koppelt veranderingen in aquatische ecosystemen op het Chinese Lössplateau aan antropogene klimaatverandering
Onderzoek koppelt veranderingen in aquatische ecosystemen op het Chinese Lössplateau aan antropogene klimaatverandering Massale evacuaties als tweede cycloon in een week voor de kust van India
Massale evacuaties als tweede cycloon in een week voor de kust van India Bossen vallen uiteen in de tropen, maar komen elders samen. Dit is wat het betekent voor dieren in het wild en het klimaat
Bossen vallen uiteen in de tropen, maar komen elders samen. Dit is wat het betekent voor dieren in het wild en het klimaat  NASA analyseert nieuwe Atlantische depressies tropische regenval
NASA analyseert nieuwe Atlantische depressies tropische regenval Landvervuiling met microplastics een onderschatte bedreiging
Landvervuiling met microplastics een onderschatte bedreiging
Hoofdlijnen
- Hoe de darmbacteriën van honingbijen helpen bij het verteren van hun stuifmeelrijke voeding
- Ontdekkingen van donkere materie kunnen licht werpen op nieuwe behandelingen voor ziekten
- Waar vindt cellulaire ademhaling plaats?
- Welke fase in meiose hervormt nucleaire membranen rond chromosomen?
- Celmembraan is naar een cel als nucleair?
- Lijst en leg de banen van RNA uit?
- Wat zijn de twee processen die ATP produceren?
- Waar vindt anaërobe ademhaling plaats?
- Waarom gebruiken wetenschappers verschillende methoden bij het onderzoeken van wetenschap?
- 3D-elektronenmicroscopie onthult de complexe ingewanden van ontziltingsmembranen

- Zo mooi als een pauw:de edelsteen voor de volgende generatie slimme sensoren

- Nieuw onderzoek naar een recent ontdekt chlorofylmolecuul kan de sleutel zijn tot betere zonnecellen

- Op zijde gebaseerde apparaten met antisense-miRNA-therapeutica kunnen de botregeneratie verbeteren

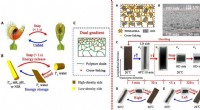
- Ontwikkeling van een ultrasnel biomimetisch snapping hydrogelmateriaal met twee gradiënten
 Waarom is de hysteresiscurve zo dik in een monster?
Waarom is de hysteresiscurve zo dik in een monster?  Facebook betaalt geen schadevergoeding voor Cambridge Analytica-zaak
Facebook betaalt geen schadevergoeding voor Cambridge Analytica-zaak Wat spelen Red Giants en Supernovas bij de productie van toekomstige sterren?
Wat spelen Red Giants en Supernovas bij de productie van toekomstige sterren?  Hoe helpen clorflora -koolstofatomen de ozon?
Hoe helpen clorflora -koolstofatomen de ozon?  Fossiel uit Utah onthult wereldwijde uittocht van zoogdieren nabij verwanten van grote continenten
Fossiel uit Utah onthult wereldwijde uittocht van zoogdieren nabij verwanten van grote continenten Hoe beïnvloedt de hoogte het plantenleven?
Hoe beïnvloedt de hoogte het plantenleven?  Hoeveel landen hebben missies in de maan gehad wanneer deze reismaan?
Hoeveel landen hebben missies in de maan gehad wanneer deze reismaan?  Hebben zuurstofstikstofstikstof koolstofboorzakken vergelijkbare fysische en chemische eigenschappen?
Hebben zuurstofstikstofstikstof koolstofboorzakken vergelijkbare fysische en chemische eigenschappen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

