
Wetenschap
Wanneer Cu en Agno3 wordt verwarmd, welke kleur geeft het waarom?
De reactie:
Koper is reactiever dan zilver. Dit betekent dat het zilver uit zijn compound kan verplaatsen. De reactie ziet er zo uit:
Cu (s) + 2Agno₃ (aq) → cu (no₃) ₂ (aq) + 2ag (s)
Wat gebeurt er:
1. Verplaatsing: De koperatomen reageren met de zilvernitraatoplossing. Koperatomen doneren elektronen aan zilverionen (Ag⁺) in de oplossing, waardoor de zilverionen neutrale zilveren atomen worden.
2. Vorming van zilver: De zilveren atomen slaan vervolgens uit de oplossing als massief zilver en vormen een glanzende, metalen coating op het koper.
3. Kopernitraat: Koperionen (Cu²⁺) gevormd in het proces lossen op in de oplossing en vormen kopernitraat (Cu (No₃) ₂).
De kleurverandering:
De sleutel tot de kleurverandering is de vorming van massief zilver:
* Aanvankelijk: De koperdraad heeft zijn typische roodbruine kleur.
* Tijdens de reactie: De zilvercoating verschijnt als een glanzende, witte/grijze laag op het koper.
* Oplossing: De oplossing, aanvankelijk kleurloos, wordt blauw als kopernitraat (Cu (No₃) ₂) vormen.
Waarom de kleur verandert ?:
De kleurverandering is te wijten aan het verschil in de manier waarop metalen licht reflecteren:
* koper: Koper weerspiegelt rode en oranje golflengten van licht, waardoor het zijn karakteristieke kleur krijgt.
* zilver: Zilver reflecteert alle golflengten van licht gelijk, waardoor het wit/grijs lijkt.
Samenvattend: Wanneer koper wordt verwarmd met zilvernitraat, treedt een chemische reactie op die zilverionen verplaatst, waardoor vast zilver en kopernitraat wordt gevormd. De zilvercoating op de koperdraad is wat de reactie zijn onderscheidende kleurverandering geeft.
 Chemici produceren een nieuw natuurenzym dat boor bevat
Chemici produceren een nieuw natuurenzym dat boor bevat  Zeer gevoelige dopaminedetector maakt gebruik van 2D-materialen
Zeer gevoelige dopaminedetector maakt gebruik van 2D-materialen Wat is een oplossing in welke alcohol als het oplosmiddel dat wordt genoemd?
Wat is een oplossing in welke alcohol als het oplosmiddel dat wordt genoemd?  Zijn organische verbindingen minder oplosbaar in water?
Zijn organische verbindingen minder oplosbaar in water?  Waarom beïnvloedt suiker het vriespunt van water?
Waarom beïnvloedt suiker het vriespunt van water?
 Is Syrië echt een klimaatoorlog? De verbanden tussen droogte, migratie en conflict
Is Syrië echt een klimaatoorlog? De verbanden tussen droogte, migratie en conflict Uit onderzoek blijkt hoe exploitanten van skitoerisme hun winsten kunnen beschermen in het licht van de klimaatverandering
Uit onderzoek blijkt hoe exploitanten van skitoerisme hun winsten kunnen beschermen in het licht van de klimaatverandering  De zondvloed:meer dan een mythe?
De zondvloed:meer dan een mythe?  Onderzoek identificeert hotspots van schendingen van de waterkwaliteit
Onderzoek identificeert hotspots van schendingen van de waterkwaliteit Biologisch afbreekbare plastic mengsels bieden nieuwe mogelijkheden voor verwijdering
Biologisch afbreekbare plastic mengsels bieden nieuwe mogelijkheden voor verwijdering
Hoofdlijnen
- Hoe Brain Mapping werkt
- Wat is een zaadlaag die niet lang ontkiemt?
- Wat regelt welke stoffen een cel binnenkomen en verlaten?
- Begrijpen hoe cellen elektrische velden volgen
- Eiwitsynthese op de oorspronkelijke aarde kan zijn gekatalyseerd door --- vóór evolutie van enzymen?
- Wat gebeurt alleen in de Gonads -mitose of meiose?
- Wat is de symbiotische relatie tussen pathogeen en een mens?
- Laat je huisdier niet per ongeluk dronken worden dit gekke seizoen (sorry Tiddles)
- Wie voert aerobe cellulaire ademhaling uit?
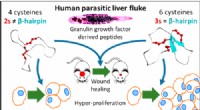
- Een molecuul geproduceerd door een Thaise leverparasiet zou de oplossing kunnen zijn voor die niet-genezende wonden
- De regels buigen:een revolutionaire nieuwe manier om metalen kneedbaar te maken

- Studie verandert lang gekoesterde concepten van celdecodering
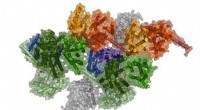
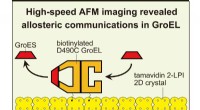
- Een chaperonine-eiwit, GroEL, heeft een complexer mechanisme dan eerder werd gedacht
- Atoombeeld van de verbazingwekkende moleculaire machines van de natuur aan het werk

 Quantum Maxwells demon teleporteert entropie uit een qubit
Quantum Maxwells demon teleporteert entropie uit een qubit Eigenaar Tesla Model 3 implanteert sleutelkaartchip in haar arm om haar voertuig te ontgrendelen en te starten
Eigenaar Tesla Model 3 implanteert sleutelkaartchip in haar arm om haar voertuig te ontgrendelen en te starten Wat gebeurt er als een koningin-mier sterft?
Wat gebeurt er als een koningin-mier sterft?  Een vliegtuig gebruiken om vluchtige organische stoffen te meten uit dagbouwinstallaties in oliezanden
Een vliegtuig gebruiken om vluchtige organische stoffen te meten uit dagbouwinstallaties in oliezanden Elektrische stroom gebruiken om bodems met een lage doorlaatbaarheid te stabiliseren
Elektrische stroom gebruiken om bodems met een lage doorlaatbaarheid te stabiliseren Vet geeft nanodeeltjes een vechtkans
Vet geeft nanodeeltjes een vechtkans Wat zou de snelheidsverandering zijn voor een voorwerp van 10 gram dat van het dak van een gebouw van 20 meter valt als het 2 seconden duurt om de grond te bereiken?
Wat zou de snelheidsverandering zijn voor een voorwerp van 10 gram dat van het dak van een gebouw van 20 meter valt als het 2 seconden duurt om de grond te bereiken?  Gebouwen in menselijk bot kunnen de sleutel zijn tot sterkere 3D-geprinte lichtgewicht structuren
Gebouwen in menselijk bot kunnen de sleutel zijn tot sterkere 3D-geprinte lichtgewicht structuren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

