
Wetenschap
Waarom behouden vloeistof en vaste stoffen hetzelfde volume?
vloeistoffen:
* constant volume: Vloeistoffen nemen de vorm van hun container aan maar weerstaan veranderingen in volume. Dit komt omdat de moleculen in een vloeistof dicht bij elkaar zijn, maar vrij kunnen bewegen. Ze hebben een vaste gemiddelde afstand tussen hen, wat resulteert in een constant volume.
* Onverwikkbaarheid: Vloeistoffen zijn bijna niet -samendrukbaar, wat betekent dat het erg moeilijk is om hun volume te veranderen door druk uit te oefenen.
vaste stoffen:
* Vaste vorm en volume: Vaste stoffen hebben een duidelijke vorm en volume. Hun moleculen zijn nauw op elkaar verpakt en strak aan elkaar gebonden, waardoor ze stijfheid en weerstand hebben tegen verandering in zowel vorm als volume.
* Compressibiliteit: Hoewel minder samendrukbaar dan gassen, kunnen vaste stoffen enigszins worden gecomprimeerd onder aanzienlijke druk.
Sleutelpunt: Het belangrijkste verschil tussen vloeistoffen en vaste stoffen in termen van volume is de bewegingsvrijheid van hun moleculen. In vloeistoffen hebben moleculen meer vrijheid om te bewegen met behoud van een constante gemiddelde afstand, terwijl vaste stoffen een vaste opstelling van moleculen hebben.
Het is echter belangrijk om te onthouden dat:
* Volumeveranderingen in vaste stoffen: Vaste stoffen kunnen kleine veranderingen in volume ervaren als gevolg van factoren zoals temperatuurveranderingen (thermische expansie/contractie) of extreem hoge druk.
* Volumeveranderingen in vloeistoffen: Vloeistoffen kunnen enigszins uitzetten wanneer ze worden verwarmd en samentrekken wanneer ze worden gekoeld, hoewel deze veranderingen over het algemeen minder significant zijn dan die in vaste stoffen.
Laat het me weten als je nog andere vragen hebt!
Hoofdlijnen
- Wat betekent classiflying in de wetenschap?
- Wat is een trans-soort sprong?
- De AlphaFold 3-upgrade maakt de voorspelling van andere soorten biomoleculaire systemen mogelijk
- Wat classificeert een vraag als wetenschappelijke vraag?
- Wat is het verschil tussen hemofilie A en B?
- Welke studie helpt je om de redenering van de redenering te begrijpen?
- Studie:Baby Kinda bavianen worden sneller onafhankelijk als moeders sociaal en dominant zijn
- Wat is de term voor uitwisseling van genetisch materiaal tussen bacteriën via contactpersonen?
- Wat gebeurt er als te veel schadelijke bacteriën het systeem binnenkomen?
- Rekenkracht lost moleculair mysterie op
- Techniek kan helpen bij massaproductie van biologisch afbreekbaar plastic

- Onderzoekers tonen aan dat een kankerverdedigingsmechanisme kan worden teruggedraaid om tumoren aan te vallen
- Onderzoekers ontwikkelen zich snel, efficiënte manier om aminozuurketens te bouwen

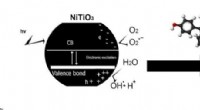
- Chemici zetten titanium nanodeeltjes om in een efficiënt wapen tegen vervuiling
 Wat is de functie van ultraviolette stralen?
Wat is de functie van ultraviolette stralen?  Wat vormde de marge van Afrika?
Wat vormde de marge van Afrika?  Nieuwe transiënte röntgenbron gedetecteerd in de melkweg NGC 4945
Nieuwe transiënte röntgenbron gedetecteerd in de melkweg NGC 4945 Wat zijn 2 redenen waarom de wetenschappelijke methode wordt gebruikt?
Wat zijn 2 redenen waarom de wetenschappelijke methode wordt gebruikt?  Wat zijn de kenmerken van een bacteriële cel?
Wat zijn de kenmerken van een bacteriële cel?  Hoe groot is een nevel?
Hoe groot is een nevel?  Waarom zou een zonsverduistering in totaal in Midden -Amerika lijken, maar niet in de Verenigde Staten?
Waarom zou een zonsverduistering in totaal in Midden -Amerika lijken, maar niet in de Verenigde Staten?  Hoe te bepalen of er een reactie was in een chemische vergelijking
Hoe te bepalen of er een reactie was in een chemische vergelijking
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


