
Wetenschap
Welke substantie heeft een sterkere aantrekkingskracht tussen zijn deeltjeswater of methaan?
Verklaring:
* waterstofbinding: Watermoleculen zijn in staat om waterstofbruggen te vormen, die sterke intermoleculaire krachten zijn. Zuurstof is zeer elektronegatief, waardoor een gedeeltelijke negatieve lading ontstaat op het zuurstofatoom en gedeeltelijke positieve ladingen op de waterstofatomen. Hierdoor kunnen watermoleculen sterke dipool-dipoolinteracties en waterstofbruggen vormen.
* methaan (CH4): Methaanmoleculen zijn niet -polair en vertonen alleen zwakke dispersiekrachten in Londen, die het zwakste type intermoleculaire kracht zijn.
Daarom leidt de sterkere waterstofbinding in water tot een significant hogere aantrekkingskracht tussen zijn moleculen in vergelijking met de zwakke Londense dispersiekrachten in methaan.
Sleutelpunten:
* Sterkere intermoleculaire krachten resulteren in hogere kookpunten, smeltpunten en oppervlaktespanning.
* Water heeft een hoger kookpunt (100 ° C) dan methaan (-161 ° C), wat de sterkere aantrekkingskrachten tussen watermoleculen weerspiegelt.
 Video:Wetenschappers onderzoeken oceaanstromingen door middel van supercomputersimulaties
Video:Wetenschappers onderzoeken oceaanstromingen door middel van supercomputersimulaties Doel voorbij winst:hoe merken het welzijn van de consument kunnen bevorderen
Doel voorbij winst:hoe merken het welzijn van de consument kunnen bevorderen  Stranden verstikt met stinkend zeewier kunnen het nieuwe normaal zijn
Stranden verstikt met stinkend zeewier kunnen het nieuwe normaal zijn Wat is een woord voor een interpretatie van observatie?
Wat is een woord voor een interpretatie van observatie?  Mountain Lion Poop
Mountain Lion Poop
Hoofdlijnen
- In welk deel van DNA is de genetische code opgeslagen?
- Welke verdeling brengt impulsen over van het centrale zenuwstelsel naar spieren of klieren?
- Hoe goede darmbacteriën het risico op hartziekten helpen verminderen
- Wetenschappers identificeren hoe de ontwikkeling van verschillende soorten dezelfde genen met verschillende kenmerken gebruikt
- Hebben zowel planten- als diercellen chloroplasten?
- Hoe de aarde verandert in verschillende ecosystemen
- Een bepaalde diersoort heeft zes paren chromosomen Hoeveel DNA -moleculen zijn deze dieren tijdens de G2 -fase aanwezig in de kernen?
- Wat doet gespecialiseerde cel?
- Welke waarde heeft de natuur? Landen hebben nu eerste richtlijnen
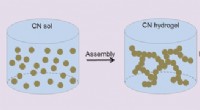
- Carbonitride-aerogels bemiddelen de fotokatalytische omzetting van water
- Een nanotech-sensor die moleculaire vingerafdrukken omzet in streepjescodes

- Nieuwe methode kan leiden tot betere in vivo medicijnafgifte

- Is lijm het antwoord op de klimaatcrisis?

- Eeuwenoud probleem opgelost met allereerste 3D-atomaire beeldvorming van een amorfe vaste stof
 Diagram van de beweging van het koelmiddel en de stroomwarmte wanneer een pomp wordt gebruikt om een gebouw te koelen?
Diagram van de beweging van het koelmiddel en de stroomwarmte wanneer een pomp wordt gebruikt om een gebouw te koelen?  Welke planeet in uw zonnestelsel heeft geen sfeer?
Welke planeet in uw zonnestelsel heeft geen sfeer?  Wat kost de meeste energie om magnetron of ex ray te genereren?
Wat kost de meeste energie om magnetron of ex ray te genereren?  Het verschil tussen woestijnplanten en regenwoudplanten
Het verschil tussen woestijnplanten en regenwoudplanten  Elektronen in kwantumvloeistof halen energie uit laserpulsen
Elektronen in kwantumvloeistof halen energie uit laserpulsen Wat gebeurt er met de energie van een naar boven gegooide bal?
Wat gebeurt er met de energie van een naar boven gegooide bal?  Wat is de vergelijking voor de reactie van salicylzuur met acetylchloride en pyridine?
Wat is de vergelijking voor de reactie van salicylzuur met acetylchloride en pyridine?  Chimpansees brengen insecten aan op wonden, een mogelijk geval van medicijngebruik?
Chimpansees brengen insecten aan op wonden, een mogelijk geval van medicijngebruik?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

