
Wetenschap
Als een reactievat 0,15 mol LIOH en 0,08 CO2 bevat, welke verbinding is het beperkende reagens?
1. Schrijf de gebalanceerde chemische vergelijking:
2 LiOH + CO₂ → Li₂co₃ + H₂o
2. Bepaal de molverhouding:
De gebalanceerde vergelijking laat zien dat 2 mol LIOH reageert met 1 mol co₂.
3. Bereken de mol Co₂ die nodig is om te reageren met alle liOH:
* Aangezien de molverhouding 2:1 is, zou u 0,15 mol LiOH / 2 =0,075 mol Co₂ nodig hebben om volledig te reageren met alle LIOH.
4. Vergelijk de beschikbare mol Co₂ met de benodigde moedervlekken:
* Je hebt 0,08 mol co₂, wat meer is dan de 0,075 mol die nodig is om met alle LIOH te reageren.
Conclusie:
Omdat je genoeg co₂ hebt om met alle liOH te reageren, is Lioh het beperkende reagens .
 Polyester verkrijgen uit plantaardige olie
Polyester verkrijgen uit plantaardige olie Welk type element verwachtte Fermi te vinden toen uranium een neutron absorbeerde?
Welk type element verwachtte Fermi te vinden toen uranium een neutron absorbeerde?  Hoe bodembacteriën kunnen beschermen tegen corrosie in staal
Hoe bodembacteriën kunnen beschermen tegen corrosie in staal  Wat is een verstoring die door vloeibare vaste stof of gas beweegt?
Wat is een verstoring die door vloeibare vaste stof of gas beweegt?  Zonne-energie omzetten in waterstofbrandstof, met hulp van fotosynthese
Zonne-energie omzetten in waterstofbrandstof, met hulp van fotosynthese
 Verschillen tussen nertsen en wezels
Verschillen tussen nertsen en wezels  Ruimtevaartorganisaties bundelen hun krachten om een globaal beeld te geven van de gevolgen van COVID-19
Ruimtevaartorganisaties bundelen hun krachten om een globaal beeld te geven van de gevolgen van COVID-19 Gewassen geteeld in Bangalore rijk aan giftige zware metalen
Gewassen geteeld in Bangalore rijk aan giftige zware metalen Hoe we de effecten van methaan meten is van belang voor het klimaatbeleid
Hoe we de effecten van methaan meten is van belang voor het klimaatbeleid Regenval in het Amazonegebied neemt toe in het natte seizoen
Regenval in het Amazonegebied neemt toe in het natte seizoen
Hoofdlijnen
- Wat is de functie van het zenuwstelsel?
- Welke groep is nauw verwant aan archabacteriën?
- Evolutie op heterdaad betrapt:wetenschappers meten hoe snel genomen veranderen
- Wanneer wordt een foetus twee cellen?
- Wat is de wetenschappelijke definitie van een virus?
- Y -vormige gebieden waar de 2 DNA -strengen scheiden?
- Hoe een 3D-dwarsdoorsnedemodel van de huid te maken
- Wat is een exparimentele groep in de wetenschap?
- Opsomming en beschrijven de verschiltakken van de wetenschap?
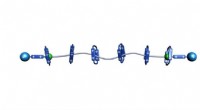
- Kleine pomp bouwt polyrotaxanen met precisie
- Het water en het zweet opzuigen - een nieuw superdroogmiddel
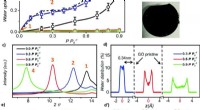
- Analyse van vingerafdrukken met synchrotron-technieken levert nieuwe inzichten op

- IJzerkatalysator kan belangrijke chemische reacties goedkoper en milieuvriendelijker maken
- Robuust MOF-materiaal vertoont selectieve, volledig omkeerbare en herhaalbare opvang van giftig atmosferisch gas

 Welke beweging vertegenwoordigt een dag waarop de aarde rond de zon beweegt?
Welke beweging vertegenwoordigt een dag waarop de aarde rond de zon beweegt?  Welke odes betekent het om samen te vatten?
Welke odes betekent het om samen te vatten?  Hoe is de wetenschap om je heen?
Hoe is de wetenschap om je heen?  Waar bestaat sfeer uit?
Waar bestaat sfeer uit?  Boeing 737 MAX-wijzigingen worden operationeel geschikt geacht:FAA
Boeing 737 MAX-wijzigingen worden operationeel geschikt geacht:FAA Is het reproductiesysteem gerelateerd aan een ander systeem?
Is het reproductiesysteem gerelateerd aan een ander systeem?  Nieuw supergeleidend qubit-testbed komt de ontwikkeling van kwantuminformatiewetenschap ten goede
Nieuw supergeleidend qubit-testbed komt de ontwikkeling van kwantuminformatiewetenschap ten goede Het landbestuur van Hawaï wil snel ontslag van beroep tegen telescoop
Het landbestuur van Hawaï wil snel ontslag van beroep tegen telescoop
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

