
Wetenschap
Wat gebeurt er wanneer zout gelijkmatig gemengd is met water?
* ontbinding: De zoutkristallen lossen op in hun individuele ionen:natriumionen (Na+) en chloride-ionen (Cl-). Dit gebeurt omdat watermoleculen polair zijn, wat betekent dat ze een enigszins positief uiteinde en een enigszins negatief einde hebben. Deze polaire moleculen trekken de geladen ionen van het zout aan, trekken ze uit elkaar en omringen ze.
* Vorming van een oplossing: De opgeloste ionen worden nu gelijkmatig over het water verspreid, waardoor een homogeen mengsel wordt gecreëerd dat een oplossing wordt genoemd.
* toename van de geleidbaarheid: Door de aanwezigheid van de ionen in de oplossing kan het elektriciteit leiden. Puur water is een slechte geleider, maar het toevoegen van zout maakt het een veel betere geleider.
* verlagen van het vriespunt: Het toevoegen van zout aan water verlaagt de temperatuur waarbij het bevriest. Dit is de reden waarom zout wordt gebruikt op wegen en trottoirs om ijs te smelten.
* Raising of Boiling Point: Het kookpunt van water wordt ook verhoogd wanneer zout wordt toegevoegd. Daarom wordt zout gebruikt bij het koken om de temperatuur van kokend water te verhogen.
* Veranderingen in osmotische druk: De aanwezigheid van opgeloste ionen verandert de osmotische druk van de oplossing, die belangrijk kan zijn in biologische systemen.
Over het algemeen, wanneer zout gelijkmatig wordt gemengd met water, lost het op en creëert het een zoute oplossing met verschillende fysische en chemische eigenschappen dan zuiver water.
 Welk volume gas wordt geproduceerd door suiker van 4 gram?
Welk volume gas wordt geproduceerd door suiker van 4 gram?  Wat is het eindproduct van fotosynthese?
Wat is het eindproduct van fotosynthese?  Wat zijn de fluorverbindingen?
Wat zijn de fluorverbindingen?  Onderzoekers ontwikkelen biologisch afbreekbare polymeren die traceerbaar zijn zonder giftige contrastmiddelen
Onderzoekers ontwikkelen biologisch afbreekbare polymeren die traceerbaar zijn zonder giftige contrastmiddelen  Hoeveel zuurstofatomen en koolstof heeft een molecuul of dioxide?
Hoeveel zuurstofatomen en koolstof heeft een molecuul of dioxide?
 Hoe beslissingen over landgebruik de productiviteit van gewassen beïnvloeden
Hoe beslissingen over landgebruik de productiviteit van gewassen beïnvloeden  De impact van deeltjesvervuiling varieert sterk, afhankelijk van waar het vandaan komt
De impact van deeltjesvervuiling varieert sterk, afhankelijk van waar het vandaan komt Welke factoren spelen een rol bij de kosten van zonnepanelen?
Welke factoren spelen een rol bij de kosten van zonnepanelen?  Als we in 2060 leefbare steden willen, moeten we samenwerken om stedelijke systemen te transformeren
Als we in 2060 leefbare steden willen, moeten we samenwerken om stedelijke systemen te transformeren Hoe wordt een Liana -wijnstok aangepast aan het regenwoud?
Hoe wordt een Liana -wijnstok aangepast aan het regenwoud?
Hoofdlijnen
- De reden voor het kleuren van een exemplaar op de microscoop
- Welke structuur wordt voornamelijk aangetroffen in planten en bacteriën?
- Waar komt fotosynthese voor en in welk deel van de cel?
- Wat is menselijk klonen?
- Wat betekent dat huidstamcellen alleen andere cellen kunnen produceren?
- Wat wordt een firtelized ei 1A fruit 2a zaad 3a blad?
- Waar werken en wonen wetenschappers?
- Welke monosacharide is een bouwsteen van de muur van de plantencel?
- Zeldzaam museumexemplaar onthult nieuwe inzichten in hoe trilobieten zichzelf tot een bal krulden
- De nieuwste magnesiumstudies maken de weg vrij voor nieuwe biomedische materialen
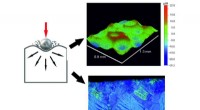
- Onderzoekers ontwerpen sensoren om plantenhormonen snel te detecteren
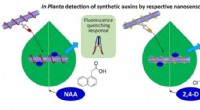
- Portretten van fijnstof
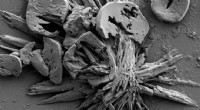
- Wetenschappers gebruiken nieuwe methode om veelbelovend batterijmateriaal te maken
- Naar kosteneffectieve oplossingen voor de volgende generatie consumentenelektronica, elektrische voertuigen en elektriciteitsnetten
 Waarom wordt de Calvin-cyclus als een donkere reactie beschouwd?
Waarom wordt de Calvin-cyclus als een donkere reactie beschouwd?  Explosieve oorsprong van secundair ijs en sneeuw
Explosieve oorsprong van secundair ijs en sneeuw Waarom heeft Ra een zonneschijf op zijn hoofd?
Waarom heeft Ra een zonneschijf op zijn hoofd?  Hoe is het klimaat in Klondike?
Hoe is het klimaat in Klondike?  Alle beweging is relatief ten opzichte van een referentiekader Wat de referentie voor zonsondergang?
Alle beweging is relatief ten opzichte van een referentiekader Wat de referentie voor zonsondergang?  Het Higgsdeeltje had het universum inmiddels kunnen beëindigen – dit is de reden waarom we nog steeds hier zijn
Het Higgsdeeltje had het universum inmiddels kunnen beëindigen – dit is de reden waarom we nog steeds hier zijn  Onderzoekers leggen de unieke onderliggende atomaire structuur van PNCP-metaalglas uit
Onderzoekers leggen de unieke onderliggende atomaire structuur van PNCP-metaalglas uit Welk soort element combineert in covalente binding?
Welk soort element combineert in covalente binding?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

