
Wetenschap
Hoeveel zuur is nodig om pH -niveau11.2 te neutraliseren?
* Het volume van de oplossing: De benodigde hoeveelheid zuur zal recht evenredig zijn met het volume van de oplossing.
* Het specifieke zuur: Verschillende zuren hebben verschillende sterke punten (dissociatieconstanten, KA), wat betekent dat ze verschillende hoeveelheden nodig hebben om neutralisatie te bereiken.
* De gewenste definitieve pH: Wil je het volledig neutraliseren naar pH 7, of naar een specifieke pH -waarde brengen?
Hier is hoe u dit probleem kunt benaderen:
1. Identificeer het specifieke zuur: Kies een zuur dat u wilt gebruiken voor neutralisatie. Gemeenschappelijke keuzes omvatten zoutzuur (HCL), zwavelzuur (H2SO4) of azijnzuur (CH3COOH).
2. Bereken de concentratie van hydroxide-ionen (OH-) in de oplossing:
* Gebruik de formule:poh =14 - pH
* Bereken POH =14 - 11.2 =2.8
* Bereken [oh-] =10^-2.8 mol/l
3. Bepaal de benodigde hoeveelheid zuur:
* Beschouw de stoichiometrie van de neutralisatiereactie tussen uw gekozen zuur en hydroxide -ionen.
* Als u bijvoorbeeld HCl (sterk zuur) gebruikt:
* HCl + OH- → H2O + Cl-
* De reactie vereist een 1:1 molverhouding van HCl tot OH-.
* Bereken de mol OH- aanwezig in de oplossing door de concentratie met het volume te vermenigvuldigen.
* Het aantal benodigde mol zuur zal hetzelfde zijn als de mol OH- aanwezig.
4. Mol zuur omzetten in de gewenste meeteenheid (gram, ml, enz.):
* Gebruik de molaire massa van het zuur en de concentratie ervan om mol om te zetten in de gewenste eenheid.
Voorbeeld:
Stel dat u 500 ml oplossing heeft met pH 11.2 en deze wilt neutraliseren met HCl om pH 7 te bereiken.
1. [OH-] =10^-2,8 mol/L =0,00158 mol/l
2. mol OH- =0.00158 mol/L * 0,5 L =0,00079 mol
3. Aangezien de reactie 1:1 is, heeft u 0,00079 mol HCl nodig
4. Uitgaande van een 1 m HCl -oplossing:
* Volume van HCl nodig =0,00079 mol / 1 mol / l =0,00079 L =0,79 ml
Belangrijke opmerking: Dit is een vereenvoudigde verklaring. In de praktijk moet u altijd zorgvuldig rekening houden met veiligheidsmaatregelen, geschikte verdunningsprocedures en het gebruik van indicatoren om het neutralisatieproces te controleren. Het wordt altijd aanbevolen om een chemicus of gekwalificeerde professional te raadplegen voor richtlijnen voor zure-base neutralisatieprocedures.
 Hoe verplaatsen rondwormen?
Hoe verplaatsen rondwormen?  Studie onthult trends van oppervlaktewaterlichaam in de VS gedurende drie decennia
Studie onthult trends van oppervlaktewaterlichaam in de VS gedurende drie decennia Wetenschappers stellen vast hoe verzuring van de oceaan koraalskeletten verzwakt
Wetenschappers stellen vast hoe verzuring van de oceaan koraalskeletten verzwakt De voedselsystemen van steden veranderen om de CO2-uitstoot te verminderen
De voedselsystemen van steden veranderen om de CO2-uitstoot te verminderen Na de lekkage van Deepwater Horizon:welke dieren hebben de ramp doorstaan?
Na de lekkage van Deepwater Horizon:welke dieren hebben de ramp doorstaan?
Hoofdlijnen
- Waarom werden dieren uitgevonden?
- Wat is de wetenschappelijke classificatie van Tulsi Tree?
- Wat betekent replicatie in de biologie?
- Hoe manukahoning infecties helpt bestrijden
- Wat zijn de functies en organen van het integumentumsysteem?
- Hoe voorkomen planten zelfbevruchting?
- Uit onderzoek blijkt dat menselijk geluid een negatieve invloed heeft op de overleving en voortplanting van krekels
- Welke structuur rond de plantencel voorkomt dat ze te veel water scheuren?
- Wat is de beste manier om te bepalen of een cel van plant of dier komt?
- Ammoniak breken:een nieuwe katalysator om bij lage temperaturen waterstof te maken uit ammoniak

- Een nieuwe composiet voor treksterkte
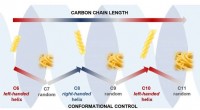
- Koolstofketens nemen fusilli- of spaghetti-vormen aan als ze oneven of even getallen hebben
- Wetenschappers ontwikkelen duurzaam materiaal voor flexibele kunstspieren

- Een nieuwe manier om opeenvolgingen van chemische reacties te automatiseren
 In de verbinding CH3F zit een fluoratoom?
In de verbinding CH3F zit een fluoratoom?  Waarom is de zon -ultieme energiebron voor alle levende wezens?
Waarom is de zon -ultieme energiebron voor alle levende wezens?  Het verschijnen van vaste metalen kan worden beschreven als?
Het verschijnen van vaste metalen kan worden beschreven als?  Door astronauten teruggevonden maansteen is waarschijnlijk van de aarde afkomstig
Door astronauten teruggevonden maansteen is waarschijnlijk van de aarde afkomstig Zijn er alle materie samen uit mengselelementen en verbindingen?
Zijn er alle materie samen uit mengselelementen en verbindingen?  Welke houding maakt een wetenschapper in staat om nieuwe en verschillende ideeën te accepteren?
Welke houding maakt een wetenschapper in staat om nieuwe en verschillende ideeën te accepteren?  In Mexico-Stad, experts vinden botten van tientallen mammoeten
In Mexico-Stad, experts vinden botten van tientallen mammoeten Experimentresultaten bevestigen anomalie, kunnen wijzen op nieuw elementair deeltje
Experimentresultaten bevestigen anomalie, kunnen wijzen op nieuw elementair deeltje
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

