
Wetenschap
Maakt CO2 een moleculaire vaste stof?
* moleculaire vaste stoffen worden gevormd door moleculen bij elkaar gehouden door intermoleculaire krachten (zoals van der Waals -krachten of waterstofbinding). Deze krachten zijn relatief zwak.
* Covalente netwerk Solids worden gevormd door atomen die aan elkaar zijn gekoppeld door een continu netwerk van sterke covalente bindingen.
In het geval van CO2:
* Elk koolstofatoom in CO2 vormt dubbele bindingen met twee zuurstofatomen.
* Deze bindingen zijn sterke covalente bindingen.
* De resulterende CO2 -moleculen hebben een lineaire vorm en ze interageren alleen met elkaar door zwakke Van der Waals -krachten.
* Bij zeer lage temperaturen (onder -78 ° C) rangschikken CO2 -moleculen echter in een specifieke, geordende structuur waarbij de koolstofatomen aan elkaar zijn gekoppeld door zwakke Van der Waals -krachten. Deze opstelling wordt nog steeds beschouwd als een moleculaire vaste stof, maar het is niet de typische toestand van CO2 bij kamertemperatuur.
Hoewel CO2 een moleculaire vaste stof vormt bij zeer lage temperaturen, wordt deze daarom nauwkeuriger beschreven als een covalent netwerk solid Bij kamertemperatuur als gevolg van de sterke covalente bindingen binnen de CO2 -moleculen.
 Wat zijn de soorten staal 4140?
Wat zijn de soorten staal 4140?  Nieuwe methodologie helpt bij het bestuderen van veelbelovende gerichte steigers voor medicijnafgifte
Nieuwe methodologie helpt bij het bestuderen van veelbelovende gerichte steigers voor medicijnafgifte Wat zijn de twee belangrijkste componenten van een atoom?
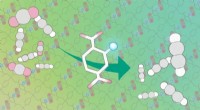
Wat zijn de twee belangrijkste componenten van een atoom?  Waarom reageert quinuclidine sneller dan triethylamine met isopropylchloride in een SN2-reactie?
Waarom reageert quinuclidine sneller dan triethylamine met isopropylchloride in een SN2-reactie?  Hoeveel sigmabindingen zitten er in propaan?
Hoeveel sigmabindingen zitten er in propaan?
 Wetenschappers vinden dat complex terrein de vorming van nevel en de meteorologische feedback ervan verergert
Wetenschappers vinden dat complex terrein de vorming van nevel en de meteorologische feedback ervan verergert Wat is de botanische naam van afval?
Wat is de botanische naam van afval?  Krachtig, lokale verhalen kunnen ons inspireren om actie te ondernemen tegen klimaatverandering
Krachtig, lokale verhalen kunnen ons inspireren om actie te ondernemen tegen klimaatverandering Het opbrengstpotentieel van tarwe die wordt geteeld in verticale boerderijen met gecontroleerde omgeving
Het opbrengstpotentieel van tarwe die wordt geteeld in verticale boerderijen met gecontroleerde omgeving Zeegras zijn recht geven
Zeegras zijn recht geven
Hoofdlijnen
- Welk voordeel zou een organisme hebben als het bepaalde genen zou kunnen in- of uitschakelen als reactie op bepaalde omstandigheden?
- Is het waar of onwaar, de micro -organismen kunnen nuttig zijn?
- Wat zijn de evolutiefasen?
- Welk idee van Darwins op basis van fossielen en de moderne organismen die hij in feite heeft gevonden, zegt in feite dat genetica -veranderingen door latere generaties worden geërfd?
- Onderzoeker onderzoekt waarom nakomelingen van oudere ouders de levensduur hebben verkort
- Hoe eiwitten in gist communiceren om partners te vinden
- Wat is de belangrijkste functie van oksel?
- Een nieuw begrip van hoe glucose je dik maakt
- Hoe verschillen Rickettsiae van Chlamydiae?
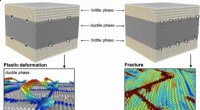
- Voorgestelde technische methode kan gebouwen en bruggen veiliger maken
- Draagbaar apparaat verlicht de weg naar betere detectie van door voedsel overgedragen ziekten

- Grote druppelsortering nu mogelijk bij hoge snelheden

- Tegengestelde actie zou de industriële gasscheiding kunnen verbeteren
- Duurzame coating doodt het COVID-virus en andere ziektekiemen in enkele minuten

 Wat zit er in een vlam? Het verrassende mysterie van hoe roet ontstaat
Wat zit er in een vlam? Het verrassende mysterie van hoe roet ontstaat  Onderzoekers ontwikkelen, nanovaccin testen om te beschermen tegen het griepvirus
Onderzoekers ontwikkelen, nanovaccin testen om te beschermen tegen het griepvirus NASA kijkt naar het Louisiana-deltasysteem, ogen wereldwijde voorspellingen
NASA kijkt naar het Louisiana-deltasysteem, ogen wereldwijde voorspellingen Onderzoekers beschrijven het gedrag van nanodeeltjes in vivo
Onderzoekers beschrijven het gedrag van nanodeeltjes in vivo Ingenieurs 3D printen zeer sterk aluminium, los eeuwenoud lasprobleem op met nanodeeltjes
Ingenieurs 3D printen zeer sterk aluminium, los eeuwenoud lasprobleem op met nanodeeltjes Wat is 101.4 Fahrenheit?
Wat is 101.4 Fahrenheit?  Wat zijn de acht meest voorkomende elementen in continentale korst?
Wat zijn de acht meest voorkomende elementen in continentale korst?  Functioneren twee eiwitten met vergelijkbare aminozuursequenties, zelfs als ze geïsoleerd zijn van verschillende organismen?
Functioneren twee eiwitten met vergelijkbare aminozuursequenties, zelfs als ze geïsoleerd zijn van verschillende organismen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

