
Wetenschap
Wat vormt zich als er iets in een vloeistof wordt opgelost?
* SOLUTE: De stof die wordt opgelost (bijv. Suiker, zout)
* oplosmiddel: De vloeistof die het oplossen doet (bijv. Water)
* Oplossing: Het homogene mengsel gevormd door de opgeloste opgeloste stof en het oplosmiddel.
Hier is hoe het werkt:
1. Oplossing: De opgeloste deeltjes breken uit elkaar en worden omringd door oplosmiddelmoleculen. Dit proces wordt aangedreven door de aantrekkelijke krachten tussen de opgeloste en oplosmiddelmoleculen.
2. Homogeniteit: De resulterende oplossing is homogeen, wat betekent dat de opgeloste deeltjes gelijkmatig over het oplosmiddel zijn verdeeld. Dit betekent dat de oplossing overal dezelfde eigenschappen heeft.
Voorbeelden:
* Suiker in water: Suiker lost op in water en vormt een suikeroplossing.
* zout in water: Zout lost op in water en vormt een zoutoplossing.
* thee: Theebladeren worden opgelost in heet water en vormen een thee -oplossing.
Belangrijke opmerking: Niet alle stoffen lossen op in alle vloeistoffen. Het vermogen van een stof om op te lossen in een bepaalde vloeistof hangt af van de aard van de opgeloste stof en het oplosmiddel. Olie lost bijvoorbeeld niet op in water, maar het lost wel op in benzine.
 Vluchten verstoord omdat vulkaan Bali uit torenhoge askolom schiet
Vluchten verstoord omdat vulkaan Bali uit torenhoge askolom schiet Hoe mensen steden en voorsteden waarnemen is niet louter een kwestie van grenslijnen
Hoe mensen steden en voorsteden waarnemen is niet louter een kwestie van grenslijnen  Kunnen dikhoorns, een kogeltrein en een enorm zonnepark naast elkaar bestaan in de Mojave-woestijn?
Kunnen dikhoorns, een kogeltrein en een enorm zonnepark naast elkaar bestaan in de Mojave-woestijn?  Hoe duurzame landbouw de wereld kan redden
Hoe duurzame landbouw de wereld kan redden Wat is bobtailing wat betreft FES?
Wat is bobtailing wat betreft FES?
Hoofdlijnen
- Wat zijn slechte dingen die nucleus doen?
- Waarom classificeren wetenschapper levende wezens?
- Hoe ontstaan genetische aandoeningen bij mensen?
- Wat produceren chondroblasten?
- Hoe heet een plantenexpert?
- Heeft nucleaire deling plaatsgevonden in mitose of intrphase?
- Wat zijn biotische factoren die de structuur van biologische gemeenschappen kunnen beïnvloeden?
- Waarom is vertaling afhankelijk van transcriptie?
- Hoe planten microben benutten om voedingsstoffen binnen te krijgen
- 2D-kristallen die voldoen aan 3D-curven veroorzaken spanning voor technische kwantumapparaten

- Nieuw onderzoek levert supersterke aluminiumlegering op

- Covalente modificatiecascade na assemblage van zelf-geassembleerde supramoleculaire structuren
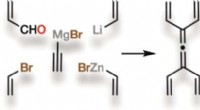
- Gespannen, symmetrisch, en nieuw:tetravinylalleen, een klein maar krachtig molecuul, is voor het eerst gesynthetiseerd
- Bananenplantenextract kan de sleutel zijn tot romiger, langer houdbaar ijs

 Hoe lang is de rotatietijd voor de planeten?
Hoe lang is de rotatietijd voor de planeten?  Lasergestuurde deeltjesversneller die paren elektronenbundels met verschillende energieën kan genereren
Lasergestuurde deeltjesversneller die paren elektronenbundels met verschillende energieën kan genereren Is de aarde en de zon dezelfde grootte?
Is de aarde en de zon dezelfde grootte?  Moleculaire chaos ten grondslag aan batterijstoring
Moleculaire chaos ten grondslag aan batterijstoring Lossen verschillende kleuren sneller op dan anderen?
Lossen verschillende kleuren sneller op dan anderen?  Wat gebeurt er ondergronds tijdens hydrofracturering?
Wat gebeurt er ondergronds tijdens hydrofracturering? Lente-irrigatie kan hittegolven in de zomer verminderen
Lente-irrigatie kan hittegolven in de zomer verminderen  China begroet Trumps ZTE olijftak voorafgaand aan handelsbesprekingen
China begroet Trumps ZTE olijftak voorafgaand aan handelsbesprekingen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

