
Wetenschap
Chemie -modelvragen van plus één?
chemie -modelvragen voor plus één (graad 11)
Hier zijn enkele modelvragen over verschillende gebieden van chemie voor plus één. Vergeet niet dat de specifieke onderwerpen en het moeilijkheidsniveau afhangen van uw curriculum.
1. Basisconcepten van chemie:
* Definieer de volgende termen:
* Wrat
* Molaire massa
* Avogadro's nummer
* Empirische formule
* Moleculaire formule
* Bereken de molaire massa van:
* Glucose (C6H12O6)
* Zwavelzuur (H2SO4)
* Bepaal de empirische formule van een verbinding met 40% koolstof, 6,7% waterstof en 53,3% zuurstof door massa
* Bereken het aantal mol en moleculen in 250 g natriumchloride (NaCl).
* Leg het verschil uit tussen een homogeen en heterogeen mengsel.
2. Structuur van atoom:
* vermeld de postulaten van het atomaire model van Bohr.
* Beschrijf de verschillende soorten subatomaire deeltjes met hun eigenschappen.
* Leg het concept van atoomnummer en massanummer uit.
* Schrijf de elektronische configuraties van de volgende elementen:
* Natrium (NA)
* Chloor (CL)
* Calcium (CA)
* Leg het belang uit van kwantumnummers bij het beschrijven van een elektron.
* Beschrijf het AUFBAU -principe, Hund's Rule en Pauli Exclusion Principle.
3. Classificatie van elementen en periodiciteit in eigenschappen:
* Beschrijf de moderne periodieke wet en leg de periodieke trends uit in:
* Atomische straal
* Ionisatie -enthalpie
* Elektronenaffiniteit
* Elektronegativiteit
* Leg het verschil uit tussen ionisatie -enthalpie en elektronenaffiniteit.
* Wat zijn de S-, P-, D- en F -blokken in de periodiek systeem?
* Voorspel de eigenschappen van een element op basis van zijn positie in de periodieke tabel.
* Bespreek het gebruik van edelgassen.
4. Chemische binding en moleculaire structuur:
* Definieer de verschillende soorten chemische bindingen:
* Ionische binding
* Covalente binding
* Metallische binding
* Waterstofbinding
* Leg de vorming van ionische en covalente bindingen uit met voorbeelden.
* Beschrijf de VSEPR -theorie en gebruik deze om de vormen van moleculen te voorspellen.
* Wat zijn de factoren die de sterkte van een covalente binding beïnvloeden?
* Leg het verschil uit tussen Sigma- en Pi -bindingen.
* Bespreek het concept van hybridisatie en zijn rol bij het binden.
5. Staten van materie:
* Beschrijf de verschillende toestanden van materie en hun karakteristieke eigenschappen.
* Leg de kinetische moleculaire theorie van gassen uit.
* Definieer de volgende termen:
* Druk
* Volume
* Temperatuur
* Boyle's wet
* De wet van Charles
* De wet van Avogadro
* Bereken het volume van een gas bij STP met behulp van de ideale gasvergelijking.
* Leg het concept van intermoleculaire krachten uit.
6. Thermodynamica:
* Definieer de volgende termen:
* Systeem
* Omgeving
* Interne energie
* Enthalpy
* Entropie
* Gibbs gratis energie
* vermeld de eerste wet van de thermodynamica en de toepassingen ervan.
* Bereken de enthalpiewijziging van een reactie met behulp van de wet van Hess.
* Leg de spontaniteit uit van een reactie op basis van Gibbs -vrije energie.
* Bespreek de factoren die de spontaniteit van een reactie beïnvloeden.
7. Evenwicht:
* Definieer de volgende termen:
* Evenwichtsconstante
* Le Chatelier's principe
* Homogeen evenwicht
* Heterogeen evenwicht
* Schrijf de evenwichtsconstante uitdrukkingen voor verschillende reacties.
* Voorspel de richting van een verschuiving in evenwicht met behulp van het principe van Le Chatelier.
* Bespreek het belang van evenwicht bij chemische reacties.
8. Redox -reacties:
* Definieer oxidatie en reductie.
* Leg het concept van oxidatienummer en zijn regels uit.
* Balans redox-reacties met behulp van de halfreactiemethode.
* Beschrijf de toepassingen van redoxreacties in het dagelijks leven.
9. Waterstof:
* Bespreek de positie van waterstof in het periodiek systeem.
* Beschrijf de verschillende isotopen van waterstof.
* Leg de voorbereiding, eigenschappen en het gebruik van waterstof uit.
* Wat zijn de milieuproblemen geassocieerd met waterstofproductie?
10. S-blokselementen:
* Beschrijf de algemene kenmerken van S-Block-elementen.
* Bespreek de trends in de chemische reactiviteit van alkali -metalen en alkalische aardmetalen.
* Leg de voorbereiding, eigenschappen en het gebruik van natrium en calcium uit.
* Wat zijn de belangrijke verbindingen van S-block-elementen en hun toepassingen?
11. P-block-elementen:
* Beschrijf de algemene kenmerken van p-block-elementen.
* Bespreek de trends in de chemische reactiviteit van halogenen en edelgassen.
* Leg de voorbereiding, eigenschappen en het gebruik van chloor en zuurstof uit.
* Wat zijn de belangrijke verbindingen van p-block-elementen en hun toepassingen?
12. Organische chemie - enkele basisprincipes en technieken:
* Definieer de volgende termen:
* Organische chemie
* Functionele groep
* Isomerisme
* Homologe serie
* Leg het concept van hybridisatie uit in organische verbindingen.
* Beschrijf het IUPAC -nomenclatuursysteem voor het benoemen van organische verbindingen.
* Bespreek de verschillende soorten isomerisme in organische verbindingen.
* Leg de basisprincipes van organische reacties uit:
* Toevoegingreactie
* Vervangingsreactie
* Eliminatiereactie
13. Koolwaterstoffen:
* classificeren koolwaterstoffen op basis van hun structuur.
* Beschrijf de voorbereiding, eigenschappen en gebruik van alkanen, alkenen en alkynes.
* Leg het concept van verbranding van koolwaterstoffen uit.
* Bespreek de milieu -impact van koolwaterstoffen.
Dit zijn slechts enkele voorbeelden van de soorten vragen die u zou kunnen tegenkomen in een plus één chemie -examen. Zorg ervoor dat je de syllabus grondig bestudeert en oefent het oplossen van problemen van schoolboeken en vroegere artikelen om vertrouwen te krijgen. Succes!
Hoofdlijnen
- Het moleculaire schild:hoe theeplanten droogte bestrijden door eiwitfosforylering
- Wat is Nadph in fotosynthese?
- Science Fair-projecten met nagellak
- Maak kennis met de vrouwen die jagen op gigantische pythons die alles opeten in de Everglades
- Wat is landbouwbiotechnologie? | Hoe dingen werken
- Wat moet een bacteriecel hebben om delen van zijn chromosoom een andere cel over te dragen?
- Wat hebben alle levende organismen gemeen?
- Wie doet wat op Wikipedia?
- Wat zijn wetenschappelijke woorden die beginnen met C?
- Dynamisch 3D-printproces met lichtgestuurde draai
- Een nieuw type chemische binding:de ladingsverschuivingsbinding

- Video:Kunnen we oceaanwater drinkbaar maken – en zouden we dat ook moeten doen?

- Tussenlagen helpen perovskietkristallisatie voor hoogwaardige light-emitting diodes

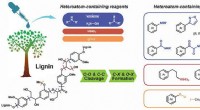
- Rassen van gefunctionaliseerde aromaten uitgebreid door heteroatoom-deelgenomen ligninesplitsing
 Hoe verhouden milieu en vrede zich tot elkaar?
Hoe verhouden milieu en vrede zich tot elkaar?  Waarom is er heel weinig licht op de bosbodem?
Waarom is er heel weinig licht op de bosbodem?  Onderzoek wijst uit dat drones en robotauto's moeten worden beschermd tegen cyberaanvallen
Onderzoek wijst uit dat drones en robotauto's moeten worden beschermd tegen cyberaanvallen Hoe poker en andere spellen kunstmatige intelligentie helpen evolueren
Hoe poker en andere spellen kunstmatige intelligentie helpen evolueren Hawking, de man wiens hersenen de handicap overstegen
Hawking, de man wiens hersenen de handicap overstegen Slibstroom volgen voor betere afvalwaterzuivering en meer biogas
Slibstroom volgen voor betere afvalwaterzuivering en meer biogas Wat is het neerslag gevormd uit magnesiumnitraat en natriumcarbonaat?
Wat is het neerslag gevormd uit magnesiumnitraat en natriumcarbonaat?  Welke informatie over Venus heeft wetenschappers opgedaan met behulp van magnetrons?
Welke informatie over Venus heeft wetenschappers opgedaan met behulp van magnetrons?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


