
Wetenschap
Vergeleken met de snelheid van een anorganische reactie is organisch meestal?
Dit is waarom:
* bindingssterkte: Organische moleculen zijn voornamelijk afhankelijk van koolstof-koolstof- en koolstofhydrogene bindingen, die relatief sterk zijn. Het verbreken van deze bindingen vereist meer energie en vertraagt de reactie. Anorganische verbindingen hebben vaak zwakkere bindingen, wat leidt tot snellere reacties.
* reactiemechanismen: Organische reacties omvatten vaak complexe multi-steps mechanismen met tussenliggende stappen die specifieke omstandigheden (temperatuur, katalysatoren) vereisen om door te gaan. Deze complexiteit voegt tijd toe aan de algehele reactie.
* sterische hindering: Organische moleculen kunnen complexe structuren hebben met omvangrijke groepen. Deze "sterische hinder" kan de benadering van reactanten belemmeren, waardoor het voor hen moeilijk is om te botsen en te reageren.
Voorbeelden:
* verbranding: Brandend hout (een organisch materiaal) is langzamer dan brandend methaan (een anorganische verbinding).
* neutralisatie: Het neutraliseren van een sterk zuur (zoals zoutzuur) met een sterke basis (zoals natriumhydroxide) is veel sneller dan de hydrolyse van een ester (een organische reactie).
Uitzonderingen:
Hoewel over het algemeen langzamer, kunnen sommige organische reacties erg snel zijn:
* SN1- en SN2 -reacties: Deze reacties met nucleofielen kunnen zeer snel zijn, afhankelijk van het substraat en nucleofiel.
* verbranding van koolwaterstoffen: Bepaalde zeer reactieve koolwaterstoffen kunnen zeer snel branden, zoals methaan.
Over het algemeen hangt de snelheid van een reactie af van vele factoren, waaronder de specifieke reactanten, reactieomstandigheden en de aanwezigheid van katalysatoren. Hoewel anorganische reacties vaak sneller zijn, zijn er ook tal van voorbeelden van snelle organische reacties.
 Onderzoeker onderzoekt hoe koolstofdioxide kan worden omgezet in de bouwstenen voor brandstof
Onderzoeker onderzoekt hoe koolstofdioxide kan worden omgezet in de bouwstenen voor brandstof Welke moleculen worden gebruikt om koolhydraten te maken?
Welke moleculen worden gebruikt om koolhydraten te maken?  Minder zout, meer eiwit:aanpak van zuivelverwerking, milieu, duurzaamheidskwesties
Minder zout, meer eiwit:aanpak van zuivelverwerking, milieu, duurzaamheidskwesties Nieuwe bioink brengt 3D-printen van menselijke organen dichter bij de realiteit
Nieuwe bioink brengt 3D-printen van menselijke organen dichter bij de realiteit Wanneer een kaliumatoom een ion vormt, verliest het één elektron, wat is de elektrische lading van ionen?
Wanneer een kaliumatoom een ion vormt, verliest het één elektron, wat is de elektrische lading van ionen?
 Hoe we het vermogen van de natuur om sterke, sterke, lichtgewicht structurele materialen te maken, evenaren of zelfs overtreffen
Hoe we het vermogen van de natuur om sterke, sterke, lichtgewicht structurele materialen te maken, evenaren of zelfs overtreffen  Fysieke kenmerken van de woestijn Biome
Fysieke kenmerken van de woestijn Biome De gezondheids- en klimaatvoordelen van het verminderen van luchtvervuiling
De gezondheids- en klimaatvoordelen van het verminderen van luchtvervuiling Dode zone Golf van Mexico deze zomer kleiner dan gemiddeld door stormen
Dode zone Golf van Mexico deze zomer kleiner dan gemiddeld door stormen Het verschil tussen Wespen en Bees
Het verschil tussen Wespen en Bees
Hoofdlijnen
- Wat zijn de meest voorkomende ziektekiemen op scholen?
- Welke structuur vertelt u dat Euglena getoont een autotrofe is?
- Wat eenzame slakken ons kunnen vertellen over de effecten van stress op het geheugen
- Wanneer dragen de mannelijke en vrouwelijke gamete elk DNA -materiaal bij?
- Waarom analyseren wetenschappers resultaten van experimenten?
- Wanneer u uitlegt wat heeft waargenomen, leidt u af aan het classificeren?
- Nieuwe inzichten in hoe het HIV-1 envelopeiwit assembleert en opneemt
- Hoe wordt een transgene gemaakt?
- Wat is de functie van endolymfe?
- Onderzoekers passen ionenzachte landingstechniek toe voor vooruitgang in materiaalsynthese

- Giftig chroom uit water filteren

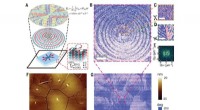
- Concentrische cirkelvormige polarisatiebanden gevonden in een ferro-elektrisch polymeer
- Een rattenbrein, aan en uit methamfetamine
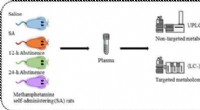
- Forensisch chemicus detecteert marihuanagebruik op basis van zweettest

 Wat is de opwaartse kracht als gevolg van vloeistofstroom rond een vliegtuigvleugel?
Wat is de opwaartse kracht als gevolg van vloeistofstroom rond een vliegtuigvleugel?  Archeologen ontdekken verloren stad die mogelijk het koninkrijk Midas . heeft veroverd
Archeologen ontdekken verloren stad die mogelijk het koninkrijk Midas . heeft veroverd Kunnen vulkaanuitbarstingen tot grote afkoeling leiden? Onderzoek wijst uit van niet
Kunnen vulkaanuitbarstingen tot grote afkoeling leiden? Onderzoek wijst uit van niet  Wat is watervrije ammoniak?
Wat is watervrije ammoniak?  Nieuw onderzoek toont verband aan tussen klimaat en het vermogen van de aarde om zichzelf aan te vullen
Nieuw onderzoek toont verband aan tussen klimaat en het vermogen van de aarde om zichzelf aan te vullen Welke verklaring beschrijft Ionische binding het beste?
Welke verklaring beschrijft Ionische binding het beste?  Handel en migratie zullen van invloed zijn op de manier waarop staten zich aanpassen aan de klimaatverandering
Handel en migratie zullen van invloed zijn op de manier waarop staten zich aanpassen aan de klimaatverandering  Welke mannen zijn het meest geassocieerd met naturalisme?
Welke mannen zijn het meest geassocieerd met naturalisme?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

