
Wetenschap
Chemische basisprincipes van waterstofbinding en eiwitten?
Chemische basis van waterstofbruggen en eiwitten:
Waterstofbinding:
Een waterstofbinding is een speciaal type dipool-dipoolinteractie dat optreedt tussen een waterstofatoom dat covalent is gebonden aan een sterk elektronegatief atoom (zoals zuurstof, stikstof of fluor) en een elektronenpaar van een ander elektronegatief atoom.
Key -functies:
* Sterkste dipool-dipool interactie: Het is sterker dan typische dipool-dipoolinteracties vanwege het hoge elektronegativiteitsverschil tussen het waterstofatoom en het elektronegatieve atoom waaraan het is gebonden.
* Zwak vergeleken met covalente bindingen: Hoewel sterker dan typische dipool-dipoolinteracties, zijn waterstofbruggen nog steeds zwakker dan covalente bindingen.
* Directioneel: De binding is directioneel, wat betekent dat deze zich vormt in een specifieke oriëntatie.
* belangrijk voor biologische systemen: Waterstofbindingen spelen een cruciale rol bij het bij elkaar houden van biologische moleculen zoals DNA, RNA en eiwitten.
eiwitten:
Eiwitten zijn grote, complexe biomoleculen die essentieel zijn voor verschillende biologische functies. Ze bestaan uit ketens van aminozuren die samen worden gekoppeld door peptidebindingen.
Rol van waterstofbruggen in eiwitten:
Waterstofbindingen spelen een cruciale rol bij het bepalen van de structuur en functie van eiwitten. Ze zijn betrokken bij:
* Secundaire structuur:
* α-helix: Waterstofbindingen vormen zich tussen de carbonylgroep van één aminozuur en de amide -waterstof van een aminozuur vier residuen vooruit in de keten, waardoor een spiraalvormige structuur wordt gevormd.
* β-plaat: Waterstofbindingen vormen zich tussen aangrenzende polypeptideketens en houden ze bij elkaar in een velachtige structuur.
* Tertiaire structuur: Interacties tussen zijketens van aminozuren, waaronder waterstofbruggen, dragen bij aan het totale driedimensionale vouw van het eiwit.
* Quaternaire structuur: Waterstofbindingen kunnen ook meerdere eiwitsubeenheden bij elkaar houden om een functioneel eiwitcomplex te vormen.
* stabiliteit en functie: Waterstofbindingen dragen bij aan de stabiliteit van de eiwitstructuur, waardoor deze zich niet ontvouwt. Ze spelen ook een rol in eiwit-eiwitinteracties, enzym-substraatinteracties en andere belangrijke biologische processen.
Specifieke voorbeelden:
* DNA: Waterstofbindingen houden de twee DNA -strengen bij elkaar, waardoor de nauwkeurige replicatie en transcriptie van genetische informatie mogelijk is.
* Water: Watermoleculen vormen waterstofbruggen met elkaar, waardoor water zijn unieke eigenschappen zoals hoog kookpunt en oppervlaktespanning krijgen.
Samenvattend:
Waterstofbindingen zijn fundamentele krachten die de structuur en functie van eiwitten beïnvloeden. Ze zijn cruciaal voor het handhaven van de stabiliteit van de eiwitstructuur, het mogelijk maken van de juiste vouwing en het faciliteren van eiwit-eiwitinteracties. Ze zijn ook betrokken bij vele andere biologische processen en benadrukken hun belang in het leven.
 Hoeveel flessen water maken 2 liter?
Hoeveel flessen water maken 2 liter?  Gegevensherinneringen van morgen:nieuwe technologie gebruiken om magneten met één molecuul in slow motion te verkennen
Gegevensherinneringen van morgen:nieuwe technologie gebruiken om magneten met één molecuul in slow motion te verkennen Welk metaal is een compound?
Welk metaal is een compound?  Hoeveel pi-bindingen zijn er aanwezig in CH3NO2?
Hoeveel pi-bindingen zijn er aanwezig in CH3NO2?  Onderzoekers ontdekken waarom E. coli sneller beweegt in siroopachtige vloeistoffen dan water
Onderzoekers ontdekken waarom E. coli sneller beweegt in siroopachtige vloeistoffen dan water
 Welke geografische systemen creëren mensen op aarde?
Welke geografische systemen creëren mensen op aarde?  Voorbereiden op extreem weer
Voorbereiden op extreem weer Baltische kokkels en wormen geven maar liefst 20 broeikasgassen vrij, 000 melkkoeien
Baltische kokkels en wormen geven maar liefst 20 broeikasgassen vrij, 000 melkkoeien Onderzoekers evalueren certificeringsprogramma's als opties voor het behoud van tropische bossen
Onderzoekers evalueren certificeringsprogramma's als opties voor het behoud van tropische bossen Infrarood NASA-beelden laten zien dat de post-tropische cycloon Emilia ten einde loopt
Infrarood NASA-beelden laten zien dat de post-tropische cycloon Emilia ten einde loopt
Hoofdlijnen
- Beschrijven cocci bacillen en spirilla schimmelvormen?
- Wat bedoel je met niet -genetische resistentie en hoe het wordt verworven?
- Hoe zijn actiereactiekrachten van toepassing op softbal?
- Morfologie is de studie van evolutionaire relaties tussen organismen?
- Een biohybride robot gemaakt van meel en haver zou kunnen fungeren als een biologisch afbreekbare vector voor herbebossing
- Welke functies zorgen ervoor dat het osmotische en pH-evenwicht in het bloed behouden blijft?
- Woestijnsprinkhanen - nieuwe risico's in het licht van klimaatverandering
- Het zit in de genen:onderzoek wijst uit hoe planten weten wanneer ze moeten bloeien
- Gameten zijn haploïd terwijl somatische cellen diploïd Wat is het verschil tussen een cel en cel?
- De zwaarste stoffen van de natuur gedecodeerd

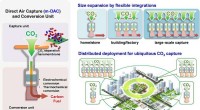
- Membranen voor het opvangen van kooldioxide uit de lucht
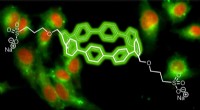
- Chemici maken circulaire fluorescerende kleurstoffen voor biologische beeldvorming
- Zeer gevoelige dopaminedetector maakt gebruik van 2D-materialen
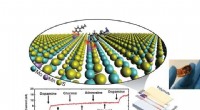
- Onderzoek naar een thermische uitdaging voor MOF's

 Als u een geschaald model van de Melkweg Galaxy zou maken, wat dan Scalig -factor zou kunnen gebruiken?
Als u een geschaald model van de Melkweg Galaxy zou maken, wat dan Scalig -factor zou kunnen gebruiken?  Studie biedt vroegste bewijs dat mensen ecosystemen veranderen met vuur
Studie biedt vroegste bewijs dat mensen ecosystemen veranderen met vuur Een kanon afgevuurd vanaf de maan is te horen op een afstand van?
Een kanon afgevuurd vanaf de maan is te horen op een afstand van?  Nanodeeltjes klikken op immuuncellen om dieper in tumoren te dringen
Nanodeeltjes klikken op immuuncellen om dieper in tumoren te dringen Verandert de juiste hemelvaart en declinatie van ster Arcturus met maand of is deze het hele jaar door hetzelfde?
Verandert de juiste hemelvaart en declinatie van ster Arcturus met maand of is deze het hele jaar door hetzelfde?  Hebben ionische verbindingen of covalente verbindingen sterkere intermoleculaire krachten?
Hebben ionische verbindingen of covalente verbindingen sterkere intermoleculaire krachten?  Welk type gas wordt gebruikt in ballonnen?
Welk type gas wordt gebruikt in ballonnen?  Probleem met implementatie van Bluetooth naar voren gebracht door team dat tracking verkent
Probleem met implementatie van Bluetooth naar voren gebracht door team dat tracking verkent
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

