
Wetenschap
Hoe verdampt een vluchtige stof sneller dan water?
Volatiliteit begrijpen
* volatiliteit verwijst naar hoe gemakkelijk een stof van een vloeistof in een gas verandert (verdampt). Het is een maat voor de neiging van een stof om te verdampen.
* intermoleculaire krachten: De sterkte van de krachten die moleculen tegen elkaar houden (zoals waterstofbruggen in water) beïnvloedt de volatiliteit. Zwakkere krachten betekenen dat moleculen gemakkelijker ontsnappen.
* dampdruk: De druk die wordt uitgeoefend door de damp boven een vloeistof is een goede indicator voor de volatiliteit. Hogere dampdruk betekent dat de stof gemakkelijk verdampt.
Waarom sommige stoffen sneller verdampen dan water
1. Zwakkere intermoleculaire krachten: Stoffen met zwakkere intermoleculaire krachten verdampen sneller. Bijvoorbeeld:
* aceton: Aceton heeft zwakkere dipool-dipoolinteracties in vergelijking met de sterke waterstofbruggen van water.
* ethanol: Ethanol heeft waterstofbindingen, maar ze zijn zwakker dan die in water.
* benzine: Benzine is een mengsel van koolwaterstoffen met zeer zwakke van der Waals -krachten.
2. Hogere dampdruk: Stoffen met hogere dampdruk verdampen sneller. Dit betekent dat ze een grotere neiging hebben om te ontsnappen in de gasfase.
voorbeelden
* aceton: Aceton verdampt gemakkelijk, waardoor een koeleffect op de huid achterblijft, omdat de zwakke krachten het laat verdampen.
* benzine: Benzine verdampt zeer snel, daarom is het zeer brandbaar.
* ether: Diethylether verdampt zo snel dat het bevriezing kan veroorzaken als het op de huid wordt aangebracht.
factoren die de verdampingssnelheid beïnvloeden
* Temperatuur: Hogere temperaturen verhogen de kinetische energie van moleculen, wat leidt tot snellere verdamping.
* oppervlakte: Een groter oppervlak legt meer vloeibare moleculen bloot aan de lucht, waardoor verdamping wordt verhoogd.
* Luchtstroom: Bewegende lucht verwijdert dampmoleculen van boven de vloeistof, waardoor er meer kan verdampen.
Key Takeaway:
De reden dat sommige stoffen sneller verdampen dan water is te wijten aan zwakkere intermoleculaire krachten en hogere dampdrukken. Deze factoren maken het voor hun moleculen gemakkelijker om te ontsnappen in de gasfase.
 Wat is een volume van een vloeistof?
Wat is een volume van een vloeistof?  Welk orbitaal wordt gevuld wanneer fluor één elektron van natrium accepteert?
Welk orbitaal wordt gevuld wanneer fluor één elektron van natrium accepteert?  Wat gebeurt er met de beweging van deeltjes als een stof wanneer het verandert van vaste vloeistof?
Wat gebeurt er met de beweging van deeltjes als een stof wanneer het verandert van vaste vloeistof?  Een stap dichter bij duurzame energie uit zeewater
Een stap dichter bij duurzame energie uit zeewater Hoeveel atomen van H zijn er in 2 mol C8H18?
Hoeveel atomen van H zijn er in 2 mol C8H18?
Hoofdlijnen
- Hoe evolutie werkt
- Welke factoren zorgen ervoor dat Filippijnse vogels met uitsterven worden bedreigd?
- De zoetwaterstroom beïnvloedt de vissen in de Everglades, maar hoe?
- Welke celonderdelen worden alleen aangetroffen in cellen van producenten?
- Je wandeling is zo duidelijk dat het diepe persoonlijkheidskenmerken kan onthullen
- Hoe de eenvoudige goudsbloem een verwoestende tomatenplaag te slim af is
- Wat zijn fotosynthetische micro-organismen?
- Het mysterie van de oorsprong van veren:hoe donzige pterosauriërs het debat opnieuw hebben aangewakkerd
- Wat zijn de vier klassen van macromoleculen en hun belang?
- PDGFR-kinaseremmer blijkt te beschermen tegen septische dood via regulering van BTLA
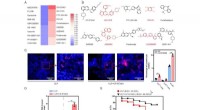
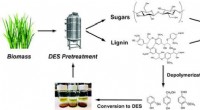
- Hernieuwbare oplosmiddelen afgeleid van lignine verlagen het afval bij de productie van biobrandstoffen
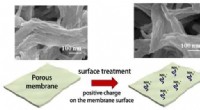
- Ontwikkeling van ultradun duurzaam membraan voor efficiënte scheiding van olie en water
- Wetenschappers krijgen atomistisch beeld van afbraak van platinakatalysator

- Hoe een bacterie de plasticvervuilingscrisis kan helpen oplossen
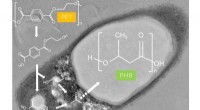
 2 manieren om ijzeraanvragen van zwavel te scheiden?
2 manieren om ijzeraanvragen van zwavel te scheiden?  Niet-ontvlambaar grafeenmembraan ontwikkeld voor veilige massaproductie
Niet-ontvlambaar grafeenmembraan ontwikkeld voor veilige massaproductie Het vriespunt van een stof is?
Het vriespunt van een stof is?  Weerstaat gips weerstand en erosie?
Weerstaat gips weerstand en erosie?  Hoe wordt neerslag weergegeven op een weerkaart?
Hoe wordt neerslag weergegeven op een weerkaart?  Centrale banken worden wakker voor de gevaren van klimaatverandering
Centrale banken worden wakker voor de gevaren van klimaatverandering Wat is het massagetal van H2o?
Wat is het massagetal van H2o?  Hoeveel elektronen zitten er in een neutraal broomatoom?
Hoeveel elektronen zitten er in een neutraal broomatoom?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

