
Wetenschap
Is het waar dat waterstofbinding een zwakke chemische aantrekkingskracht is tussen polaire moleculen?
* waterstofbruggen zijn inderdaad zwak in vergelijking met covalente bindingen. Dit komt omdat ze elektrostatische interacties met zich meebrengen in plaats van het delen van elektronen.
* waterstofbruggen zijn specifiek tussen moleculen die waterstof bevatten die zijn gebonden aan een sterk elektronegatief atoom. Dit zijn meestal zuurstof, stikstof of fluor.
* De betrokken moleculen hoeven niet polair te zijn. Hoewel waterstofbruggen vaak tussen polaire moleculen optreden, kunnen ze zich ook vormen tussen een polair molecuul en een niet -polair molecuul. De sleutel is de aanwezigheid van een waterstofatoom gebonden aan een sterk elektronegatief atoom in een van de moleculen.
Samenvattend:
* Waterstofbindingen zijn zwakke attracties.
* Ze betreffen waterstofatomen die zijn gebonden aan zeer elektronegatieve atomen.
* Ze kunnen optreden tussen polaire en niet -polaire moleculen.
Het is belangrijk op te merken dat, hoewel zwak afzonderlijk, waterstofbindingen collectief sterk kunnen zijn, een cruciale rol spelen in veel biologische processen.
 Neerslag-extremen in droge regio's van China, nauw verwant aan SST
Neerslag-extremen in droge regio's van China, nauw verwant aan SST Welk effect heeft een tornado op de geosfeer?
Welk effect heeft een tornado op de geosfeer?  Zorgen over klimaatverandering veel groter in Latijns-Amerika, Caribisch gebied dan de VS, Canada
Zorgen over klimaatverandering veel groter in Latijns-Amerika, Caribisch gebied dan de VS, Canada Wat zijn de belangrijkste kenmerken van natuurlijke hulpbronnen?
Wat zijn de belangrijkste kenmerken van natuurlijke hulpbronnen?  Welke 2 dingen zijn te vinden in de exosfeer?
Welke 2 dingen zijn te vinden in de exosfeer?
Hoofdlijnen
- Seks en macht in het dierenrijk:zeven dieren die je doen nadenken over wat je denkt te weten
- Duwen, trekken of draaien:de vele bewegingen van trilhaartjes
- Wat zijn de 16 verschillende organismen die evolutie vertegenwoordigen van cel tot mens?
- Hoe en wat horen vleermuizen?
- 10 manieren om jezelf gelukkig te maken
- Wat is de variabele die door wetenschappers wordt bestuurd?
- Wat zijn de functies van Triglyceride Phospholipid & Sterol?
- Het blootleggen van sleutelspelers op het gebied van genuitschakeling:inzichten in plantengroei en ziekten bij de mens
- Als een bacterie geen glucose kan fermenteren, waarom dan zijn vermogen niet testen op andere koolhydraten?
- Wetenschappers hebben de oorsprong van de bouwstenen van het leven ontdekt
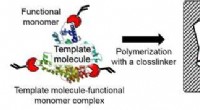
- Zeer gevoelige methode om potentiële kankerbiomarker te detecteren
- Waarom toekomstige huizen gemaakt kunnen worden van levende schimmel

- Onderzoek onthult waarom het moeilijk is om de geur uit polyester te krijgen

- Buigbaar beton en andere met koolstof doordrenkte cementmengsels kunnen de wereldwijde uitstoot drastisch verminderen

 Hoe verleng je de levensduur van smeermiddelen?
Hoe verleng je de levensduur van smeermiddelen? Hoeveel mol c zit er in 000831 co2?
Hoeveel mol c zit er in 000831 co2?  Waarom neemt de grootte van het atoom niet regelmatig af in een periode?
Waarom neemt de grootte van het atoom niet regelmatig af in een periode?  Een verbeterde methode voor het coaten van gouden nanostaafjes
Een verbeterde methode voor het coaten van gouden nanostaafjes Nieuw membraan scheidt gespiegelde moleculen efficiënt
Nieuw membraan scheidt gespiegelde moleculen efficiënt Nieuwe inzichten in hoe cyanobacteriële eiwitten koolstof in veranderende omstandigheden recycleren
Nieuwe inzichten in hoe cyanobacteriële eiwitten koolstof in veranderende omstandigheden recycleren  Watersplitsingskatalysatoren ontwerpen met behulp van afvalgistbiomassa
Watersplitsingskatalysatoren ontwerpen met behulp van afvalgistbiomassa Wat is de snelheid van geluid in 25 Celsius Air?
Wat is de snelheid van geluid in 25 Celsius Air?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

