
Wetenschap
Natriumchloride is geleider of isolator?
vaste toestand:
* ionische binding: Natriumchloride is een ionische verbinding, wat betekent dat het een kristalrooster vormt waar positief geladen natriumionen (Na+) en negatief geladen chloride-ionen (Cl-) samen worden gehouden door elektrostatische krachten.
* Vaste ionen: In de vaste toestand zijn deze ionen opgesloten in hun posities in het rooster. Ze kunnen niet vrij bewegen.
* Geen gratis ladingsdragers: Omdat de ionen niet kunnen bewegen, zijn er geen gratis ladingsdragers om elektriciteit te leiden. Daarom is solide NaCl een isolator.
opgelost in water of gesmolten:
* ionmobiliteit: Wanneer natriumchloride oplost in water, dissociëren de ionen (gescheiden) en worden omringd door watermoleculen. Deze opgeloste ionen kunnen nu vrij bewegen.
* Laad dragers: De mobiele ionen in de oplossing fungeren als ladingsdragers, waardoor elektriciteit door de oplossing kan stromen.
* geleidbaarheid: Daarom is opgelost natriumchloride een goede geleider van elektriciteit. Evenzo leidt gesmolten NaCl elektriciteit omdat de ionen vrij kunnen bewegen in de gesmolten toestand.
Samenvattend: Het vermogen van natriumchloride om elektriciteit te leiden hangt af van de bewegingsvrijheid van zijn ionen. In solide vorm zijn de ionen vast en kunnen ze niet bewegen, waardoor het een isolator is. In opgeloste of gesmolten vorm zijn de ionen vrij om te bewegen, waardoor het een geleider is.
 Het klimaat aanpassen om het te redden:wie beslist?
Het klimaat aanpassen om het te redden:wie beslist?  35% van de microplastics die in de wereldzeeën terechtkomen, is afkomstig van synthetisch textiel
35% van de microplastics die in de wereldzeeën terechtkomen, is afkomstig van synthetisch textiel Onderzoekers ontwikkelen een gelachtige vloeistof om bosbranden te voorkomen
Onderzoekers ontwikkelen een gelachtige vloeistof om bosbranden te voorkomen Nieuwe gegevens helpen recente fluctuaties in het magnetische veld van de aarde te verklaren
Nieuwe gegevens helpen recente fluctuaties in het magnetische veld van de aarde te verklaren VN vat klimaatwetenschap samen:wereld gaat de verkeerde kant op
VN vat klimaatwetenschap samen:wereld gaat de verkeerde kant op
Hoofdlijnen
- Waarom is de hypothese zo belangrijk voor de wetenschappelijke methode?
- Hoe helpt meiosis informatie van een gezonde zygote?
- Ontwikkeling van een zeer nauwkeurig computermodel van het menselijk metabolisme
- Wat wordt de naam gegeven om te verwerken wanneer mannelijke en felmale sekscellen smelten?
- Het belang van diffusie in organismen
- Onderzoekers onthullen hoe stamcellen beslissingen nemen
- In welk biome leven mensen?
- Wat voor soort cellen ontwikkelen zich uit stamcellen van Uni-potte?
- Wat zijn protosme's?
- Nieuwe methode stelt wetenschappers in staat om snel individuele virusdeeltjes te bekijken
- De breuktaaiheid van het materiaal voor vliegtuigbouw wordt 1,5 keer verhoogd

- Ingenieurs maken een eenvoudige test die stresshormonen in zweet kan meten, bloed, urine of speeksel

- Onderzoekers zien in realtime scheurvorming in 3D-geprint wolfraam

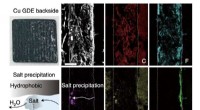
- Bifunctionele ionomeren gebruiken als elektrolyten om ethyleen uit koolstofdioxide te synthetiseren
 Onderzoek toont aan dat de impact van het griepvirus verschilt per beroep en bedrijfstak
Onderzoek toont aan dat de impact van het griepvirus verschilt per beroep en bedrijfstak Tijgers klampen zich vast aan overleving in steeds meer gefragmenteerde bossen op Sumatras
Tijgers klampen zich vast aan overleving in steeds meer gefragmenteerde bossen op Sumatras Wat zijn drie abiotische kenmerken van een ecosysteem?
Wat zijn drie abiotische kenmerken van een ecosysteem?  Hoeveel is 98,5 celsium in Fahrenheit?
Hoeveel is 98,5 celsium in Fahrenheit?  Caverns vormen zich meestal in fundament.?
Caverns vormen zich meestal in fundament.?  Lichaamsdelen van een zeemeeuw
Lichaamsdelen van een zeemeeuw Auto's worden groen en online als de Tokyo Motor Show wordt geopend
Auto's worden groen en online als de Tokyo Motor Show wordt geopend  Onverwachte historische ontdekking:overblijfselen van beroemde Sami-vrouw gevonden
Onverwachte historische ontdekking:overblijfselen van beroemde Sami-vrouw gevonden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

