
Wetenschap
Welk type binding wordt gevormd tussen een waterstof op één polair molecuul en een zeer elektronegatief atoom zoals zuurstof of stikstof een ander molecuul?
Dit is waarom:
* polariteit: Het elektronegativiteitsverschil tussen waterstof en zuurstof of stikstof creëert een polaire binding, waarbij het waterstofatoom een gedeeltelijke positieve lading (Δ+) draagt en de zuurstof of stikstof die een gedeeltelijke negatieve lading draagt (Δ-).
* Elektrostatische aantrekkingskracht: Het gedeeltelijk positieve waterstofatoom wordt aangetrokken tot het gedeeltelijk negatieve zuurstof- of stikstofatoom van een nabijgelegen molecuul. Deze aantrekkingskracht vormt de waterstofbinding.
Belangrijke opmerking: Waterstofbindingen zijn zwakker dan covalente bindingen maar zijn nog steeds significant in veel biologische en chemische processen.
 Wat heeft 82 protonen?
Wat heeft 82 protonen?  Broomatomen krijgen altijd één elektron wanneer ze een ion worden welk atoom hetzelfde aantal elektronen heeft als een broomionen?
Broomatomen krijgen altijd één elektron wanneer ze een ion worden welk atoom hetzelfde aantal elektronen heeft als een broomionen?  Wat gebeurt er als je kaliumpermanganaat met olie mengt?
Wat gebeurt er als je kaliumpermanganaat met olie mengt?  Hoe te identificeren of een oplossing neutraal, base of zuur is
Hoe te identificeren of een oplossing neutraal, base of zuur is  Gasopslagmethode kan de volgende generatie schone energievoertuigen helpen
Gasopslagmethode kan de volgende generatie schone energievoertuigen helpen
Hoofdlijnen
- Wordt de wetenschappelijke methode gebruikt om kennis te verkrijgen?
- Welk vasculair weefsel draagt voedsel van de bladeren tot wortels?
- Een geval van chimpansees of een grote uitbraak? Syndromale surveillance kan van cruciaal belang zijn
- Wat maakt urine geel? Wetenschappers ontdekken het verantwoordelijke enzym
- Hoe planten oxidatieve stress voorkomen
- Wat zijn de DNA -moleculen gevonden in celorganel?
- Welk organisme wordt gebruikt om gisting te bestuderen?
- Waarom zijn sommige mensen DNA sterker dan andere?
- Waarom de wetenschap niet helpt bij het verkopen van chocoladekoekjes
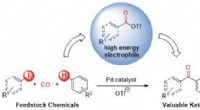
- Een groenere manier om ketonen te maken
- Wetenschappers ontdekken een nieuw complex europiumhydride

- Nieuw mogelijk doelwit voor de behandeling van veelvoorkomende ziekten

- Mixed and matched:Integratie van metaal-organische raamwerken in polymeren voor kooldioxideafscheiding

- Stereoselectieve alkeensynthese met onedele nikkelkatalyse
 Anorganische biomaterialen voor hechting van zacht weefsel
Anorganische biomaterialen voor hechting van zacht weefsel Onderzoekers 3D printen minuscule veelkleurige microstructuren
Onderzoekers 3D printen minuscule veelkleurige microstructuren Hoe is de inhoud die wordt gemaakt van dingen die nooit leefden?
Hoe is de inhoud die wordt gemaakt van dingen die nooit leefden?  Waarom ziet de constellatie Cassiopeia er vandaag anders uit?
Waarom ziet de constellatie Cassiopeia er vandaag anders uit?  Vuurwerk op 4 juli veroorzaakte het op één na hoogste niveau van luchtvervuiling sinds de vakantie in Zuid-Californië in tien jaar
Vuurwerk op 4 juli veroorzaakte het op één na hoogste niveau van luchtvervuiling sinds de vakantie in Zuid-Californië in tien jaar De kenmerken en fysieke kenmerken van een Tiger
De kenmerken en fysieke kenmerken van een Tiger Wie heeft de schuld toen iCloud werd 'gehackt':jij of Apple?
Wie heeft de schuld toen iCloud werd 'gehackt':jij of Apple?  Wat worden hulpmiddelen gebruikt om de biosfeer te bestuderen?
Wat worden hulpmiddelen gebruikt om de biosfeer te bestuderen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

