
Wetenschap
Hoe wordt NACI opgelost in water een voorbeeld van like oplost zoals?
Dit is waarom:
* polariteit: Water (H₂o) is een polair molecuul omdat het zuurstofatoom een gedeeltelijke negatieve lading heeft en zijn waterstofatomen gedeeltelijke positieve ladingen hebben. Deze ongelijke verdeling van aanklachten creëert een dipoolmoment.
* ionische binding: NaCl bestaat als een kristallijne structuur die bij elkaar wordt gehouden door ionische bindingen, wat betekent dat het bestaat uit positief geladen natriumionen (Na+) en negatief geladen chloride-ionen (Cl-).
* interactie: Wanneer NaCl wordt toegevoegd aan water, omringen de polaire watermoleculen de ionen. De gedeeltelijk negatieve zuurstofatomen in water worden aangetrokken door de positieve natriumionen en de gedeeltelijk positieve waterstofatomen worden aangetrokken door de negatieve chloride -ionen. Deze sterke elektrostatische interactie tussen de polaire watermoleculen en de geladen ionen overwint de ionische krachten die het NaCl -kristal tegen elkaar houden, waardoor het oplost.
In wezen hebben zowel water als NaCl een sterke affiniteit voor elkaar vanwege hun polaire aard, waardoor ze "like" zijn en hen kunnen oplossen.
daarentegen:
* Niet -polaire oplosmiddelen , zoals olie, hebben geen significante scheiding van lading en kan niet effectief interageren met polaire moleculen of ionen. Daarom mengen olie en water niet; Olie is niet -polair en lost niet op in water.
* Niet -polaire opgeloste stoffen (zoals vetten of oliën) zal oplosen in niet -polaire oplosmiddelen.
Dus, de "Like Lost Like" -regel helpt verklaren waarom bepaalde stoffen goed samengaan met anderen, terwijl anderen gescheiden blijven.
 Hoe bedrijven hun leveranciers krachtig kunnen wapenen om de CO2-uitstoot terug te dringen
Hoe bedrijven hun leveranciers krachtig kunnen wapenen om de CO2-uitstoot terug te dringen  Waarom is condens een belangrijk proces in de watercyclus?
Waarom is condens een belangrijk proces in de watercyclus?  Dichtheid van methyleenchloride in vergelijking met water?
Dichtheid van methyleenchloride in vergelijking met water?  Waarom verwijderen sommige alledaagse stoffen roest uit metalen?
Waarom verwijderen sommige alledaagse stoffen roest uit metalen?  Wat is de naam van de temperatuur waarop een mengsel bevriest?
Wat is de naam van de temperatuur waarop een mengsel bevriest?
 Boomsoortendiversiteit verbetert de weerstand tegen droogte in bossen
Boomsoortendiversiteit verbetert de weerstand tegen droogte in bossen Naar huis bellen? Ily vindt de vaste lijn opnieuw slimmer en gebruiksvriendelijker
Naar huis bellen? Ily vindt de vaste lijn opnieuw slimmer en gebruiksvriendelijker  De effecten van zonnevlammen op technologie
De effecten van zonnevlammen op technologie Een studie waarschuwt voor de ecologische impact van sedimentophoping in rivierlopen
Een studie waarschuwt voor de ecologische impact van sedimentophoping in rivierlopen Beschrijf de interactie tussen een plant en zijn omgeving?
Beschrijf de interactie tussen een plant en zijn omgeving?
Hoofdlijnen
- Welke F -waarde betekent in de microbiologie?
- Waar zijn bacteriofaag Lambda in?
- Microchip onthult hoe tumorcellen overgaan naar invasie
- Welke structuur is in een dierencel verantwoordelijk voor het opslaan van genetische informatie (DNA) de cel?
- De middelen waarmee biologen beantwoorden dat hun wetenschappelijke vragen worden genoemd?
- Hoe DNA gekoppeld aan de rol van ribosomen in een cel?
- Als alle sekscellen een organisme een allel genotype hebben dat moet zijn?
- Wie zijn Janssen Brothers of Biology?
- Welke van de volgende bacteriën vertoont echte beweeglijkheid op objectglaasjes bij B.cereus P.aeruginosa en S.volutans?
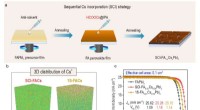
- Ontkoppeling van formamidinium–cesium perovskieten voor efficiënte fotovoltaïsche energie
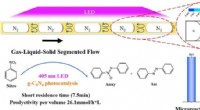
- Onderzoekers stellen een nieuwe benadering voor om heterogene fotosynthese van azoverbindingen te verbeteren
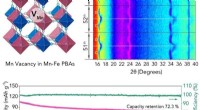
- Onderzoek maakt oplaadbare batterijen met een langere levensduur mogelijk
- Ultrasnelle elektronen in magnetische oxiden:een nieuwe richting voor spintronica?

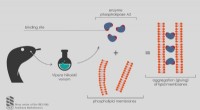
- Chemici ontdekten hoe het addergif werkt
 Cloudgegevens een zilveren randje voor voorspellingen van klimaatverandering
Cloudgegevens een zilveren randje voor voorspellingen van klimaatverandering Tatoeages op nanoschaal voor individuele cellen kunnen vroegtijdige waarschuwingen geven voor gezondheidsproblemen
Tatoeages op nanoschaal voor individuele cellen kunnen vroegtijdige waarschuwingen geven voor gezondheidsproblemen  Beste van vorig jaar:de beste Phys.org-artikelen van 2020
Beste van vorig jaar:de beste Phys.org-artikelen van 2020 Vier decennia aan gegevens klinkt vroegtijdige waarschuwing op Lake George
Vier decennia aan gegevens klinkt vroegtijdige waarschuwing op Lake George Drie jaar durende studie van jonge sterren met NASA's Hubble gaat een nieuw hoofdstuk in
Drie jaar durende studie van jonge sterren met NASA's Hubble gaat een nieuw hoofdstuk in  Origineel ontwerp Olympische Spelen wordt geveild in New York
Origineel ontwerp Olympische Spelen wordt geveild in New York Twitter gaat het beperken van reacties testen om online misbruik aan te pakken
Twitter gaat het beperken van reacties testen om online misbruik aan te pakken De VS willen over vijf jaar een bemande missie naar de maan, maar kan en moet dat?
De VS willen over vijf jaar een bemande missie naar de maan, maar kan en moet dat?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

