
Wetenschap
Waarom is magnesiumchloride mgcl2?
* magnesium (mg): Magnesium is een alkalisch aardmetaal in groep 2 van het periodiek systeem. Het heeft twee valentie -elektronen (elektronen in de buitenste schaal).
* chloor (CL): Chloor is een halogeen in groep 17 van het periodiek systeem. Het heeft zeven valentie -elektronen.
ionische binding:
1. Elektronenoverdracht: Magnesium wil zijn twee valentie -elektronen verliezen om een stabiele elektronenconfiguratie te bereiken zoals de Noble Gas Neon. Chloor daarentegen heeft nog een elektron nodig om een stabiele elektronenconfiguratie te bereiken, zoals de edelgasargon.
2. Vorming van ionen: Magnesium verliest twee elektronen en wordt een positief geladen ion (mg²⁺). Elk chlooratoom krijgt één elektron en wordt een negatief geladen ion (CL⁻).
3. Elektrostatische aantrekkingskracht: De tegengesteld geladen ionen worden tot elkaar aangetrokken door elektrostatische krachten. Deze aantrekkingskracht resulteert in de vorming van een ionische binding.
formule:
* mg²⁺ (Magnesiumion) heeft twee chloorionen (CL⁻) nodig om zijn positieve lading in evenwicht te brengen.
* Daarom is de chemische formule voor magnesiumchloride mgcl₂ .
In essentie weerspiegelt de formule mgcl₂ de gebalanceerde elektrostatische krachten tussen het magnesiumkation (mg²⁺) en twee chloride -anionen (CL⁻).
 Hoe wetenschappers vrijgegeven militaire foto's gebruiken om historische ecologische veranderingen te analyseren
Hoe wetenschappers vrijgegeven militaire foto's gebruiken om historische ecologische veranderingen te analyseren Nieuwe landbewegingskaart toont de menselijke impact op het Britse landschap
Nieuwe landbewegingskaart toont de menselijke impact op het Britse landschap Vroegere diepwaterdynamiek in de westelijke tropische Stille Oceaan
Vroegere diepwaterdynamiek in de westelijke tropische Stille Oceaan Verschil tussen varens en mossen
Verschil tussen varens en mossen Hoe een stortvloed aan lockdown-vrijwilligers de verborgen weergeschiedenis van Groot-Brittannië redde
Hoe een stortvloed aan lockdown-vrijwilligers de verborgen weergeschiedenis van Groot-Brittannië redde
Hoofdlijnen
- Hier is hoe planten- en dierencellen verschillen
- Wanneer reproductieve cellen van mannelijke en vrouwelijke planten aansluiten bij wat zal zich vormen?
- Hoe menselijk sperma echt zwemt:nieuw onderzoek daagt eeuwenoude veronderstellingen uit
- Welke verbinding begint alle drie de versies van cellulaire ademhaling?
- Hoe beïnvloedt de natuurlijke selectie polygene eigenschappen?
- Waar wordt messenger-RNA gehecht tijdens de eiwitconstructie?
- Onderzoekers brengen dramatische achteruitgang in genetische diversiteit van noordwestelijke zalm in kaart
- Hoe DNA-bewijs werkt
- Wetenschappers hebben ontdekt dat de micro-inkapselingstechniek de efficiëntie van theeboomolie verhoogt voor duurzame toepassingen
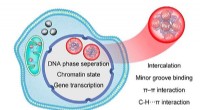
- Moleculair mechanisme van door rutheniumcomplex geïnduceerde DNA-fasescheiding onthuld
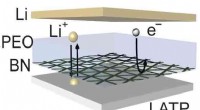
- Nieuwe techniek produceert lithiumbatterijen met een langere levensduur
- Hoogwaardige elektrokatalysatoren om de ontwikkeling van directe ethanolbrandstofcellen te stimuleren

- Virusoppervlakken helpen ingenieurs bij het bestuderen van toepassingen voor vaccins en gentherapie
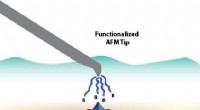
- Chemici leren hoe ze fenolen in gerookte voedselmonsters kunnen detecteren met behulp van vitamine B4

 Autoshow lijkt meer op CES dan niet
Autoshow lijkt meer op CES dan niet  Welke continenten ten oosten van Equator?
Welke continenten ten oosten van Equator?  Spaanse rechter negeert back-upsite voor betwiste Hawaii-telescoop
Spaanse rechter negeert back-upsite voor betwiste Hawaii-telescoop Zijn mannelijke genen van Mars, vrouwelijke Venus? Review benadrukt sekseverschillen in gezondheid en ziekte
Zijn mannelijke genen van Mars, vrouwelijke Venus? Review benadrukt sekseverschillen in gezondheid en ziekte  De bouwstenen voor het verkennen van nieuwe exotische toestanden van materie
De bouwstenen voor het verkennen van nieuwe exotische toestanden van materie Wat voor soort tektonische grens delen de Nazca en Caribbean -plaat?
Wat voor soort tektonische grens delen de Nazca en Caribbean -plaat?  Kunstmatige atomen creëren stabiele qubits voor quantum computing
Kunstmatige atomen creëren stabiele qubits voor quantum computing Hoe huiselijk partnergeweld de vruchtbaarheidscijfers in een kleinschalige samenleving kan beïnvloeden (bijgewerkt)
Hoe huiselijk partnergeweld de vruchtbaarheidscijfers in een kleinschalige samenleving kan beïnvloeden (bijgewerkt)
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

