
Wetenschap
Op welke manier zijn atomen van één element anders dan andere elementen?
* Aantal protonen: Het meest fundamentele verschil is het aantal protonen in de kern van het atoom. Dit nummer, het atoomnummer genoemd, definieert het element. Alle koolstofatomen hebben bijvoorbeeld 6 protonen, alle zuurstofatomen hebben 8 protonen, enzovoort.
* Aantal neutronen: Hoewel alle atomen van een bepaald element hetzelfde aantal protonen hebben, kunnen ze verschillende aantallen neutronen hebben. Dit verschil creëert isotopen, die variaties zijn van een element met verschillende atoommassa's.
* Elektronenconfiguratie: Het aantal elektronen in een atoom is meestal gelijk aan het aantal protonen en ze zijn gerangschikt in specifieke energieniveaus die elektronenschalen worden genoemd. De opstelling van elektronen in deze schalen bepaalt de chemische eigenschappen van het atoom en hoe het zal interageren met andere atomen.
* Atomische massa: De atomaire massa van een element is de gemiddelde massa van al zijn isotopen. Het wordt voornamelijk bepaald door het aantal protonen en neutronen in de kern.
Samenvattend verschillen atomen van één element van atomen van andere elementen omdat ze een uniek aantal protonen hebben, die hun atoomnummer en hun identiteit definiëren. Dit verschil in protonen leidt ook tot verschillen in hun elektronenconfiguraties, atomaire massa's en chemische eigenschappen.
 Bereid je voor op het ergste:10 stappen om je voor te bereiden op wildvuurrook
Bereid je voor op het ergste:10 stappen om je voor te bereiden op wildvuurrook Regering rangschikt 18 Amerikaanse vulkanen als zeer hoge bedreiging
Regering rangschikt 18 Amerikaanse vulkanen als zeer hoge bedreiging Wat beïnvloedt eigenlijk de luchtvervuiling boven de Indische Oceaan?
Wat beïnvloedt eigenlijk de luchtvervuiling boven de Indische Oceaan?  National Weather Service bevestigt tornado nabij Nashville
National Weather Service bevestigt tornado nabij Nashville Welk koninkrijk heeft het kleinste aantal soorten?
Welk koninkrijk heeft het kleinste aantal soorten?
Hoofdlijnen
- Het gebied van een lang bot waar lengtegroei optreedt, is het?
- Welke term beschrijft de conditie die plantencellen vereisen?
- Wat zijn de zichtbare structuren die aanwezig zijn in protistencel die geen dier- en plantencel zijn?
- Waarom gebruikte Mendel pure broodplanten?
- Waarom het presenteren van ‘slechts de feiten’ niet zal werken voor genetisch gemodificeerd voedsel
- Hoe wordt de studie van afval genoemd?
- Waarom Microscope nodig in de studie van zolaogie?
- De sites waar DNA -replicatie en scheiding plaatsvinden, worden opgeroepen?
- Waar zijn plantes van gemaakt?
- Nanocoating maakt lichtgewicht metaalschuim bothard en explosieveilig

- Focus op de zuurstofreductiereactie bij het zoeken naar efficiëntere waterstofcellen

- Menselijk afval omzetten in plastic, voedingsstoffen kunnen helpen bij ruimtereizen over lange afstanden

- Wetenschappers ontdekken verbindingen die hadden kunnen helpen bij het ontstaan van leven op aarde

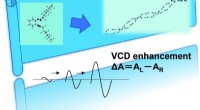
- Een nieuwe horizon voor vibrationele circulair dichroïsme spectroscopie
 Indringende vraag:Zijn de huidige kerncentrales veilig?
Indringende vraag:Zijn de huidige kerncentrales veilig?  Een filter voor schonere qubits
Een filter voor schonere qubits Tegengestelde piëzoresistente effecten van rheniumdisulfide in twee hoofdrichtingen
Tegengestelde piëzoresistente effecten van rheniumdisulfide in twee hoofdrichtingen Van chips uit het stenen tijdperk tot microchips:hoe kleine gereedschappen ons menselijk hebben gemaakt
Van chips uit het stenen tijdperk tot microchips:hoe kleine gereedschappen ons menselijk hebben gemaakt  Wat gebeurt er als er regen valt op woestijngronden? Een vernieuwd model biedt antwoorden
Wat gebeurt er als er regen valt op woestijngronden? Een vernieuwd model biedt antwoorden  Evolutie van een moordenaar:hoe Afrikaanse Salmonella de sprong maakte van de darm naar de bloedbaan
Evolutie van een moordenaar:hoe Afrikaanse Salmonella de sprong maakte van de darm naar de bloedbaan  Wat is de klimatologische zone waarin Tundra Tegion is gevonden?
Wat is de klimatologische zone waarin Tundra Tegion is gevonden?  Hoe kan een fabriek schadelijk zijn voor de levende organismen?
Hoe kan een fabriek schadelijk zijn voor de levende organismen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

