
Wetenschap
Als 0,1 concentratie van HCl hoeveel pH?
Inzicht in de concepten
* HCl (zoutzuur): Een sterk zuur, wat betekent dat het volledig ioniseert in water. Dit betekent dat een 0,1 M HCl -oplossing 0,1 m H+ -ionen zal produceren.
* pH: Een maat voor de zuurgraad of alkaliteit van een oplossing. Het wordt berekend met behulp van de volgende formule:
pH =-log [H+]
waarbij [H+] de concentratie van waterstofionen in mol is per liter (M).
Berekening
1. Identificeer de H+ -concentratie: Omdat HCl een sterk zuur is en volledig ioniseert, is de [H+] -concentratie gelijk aan de initiële HCL -concentratie, die 0,1 M is.
2. Sluit de [H+] aan op de pH -formule:
pH =-log (0,1)
3. Bereken de pH:
pH =1
Daarom heeft een 0,1 M HCl -oplossing een pH van 1.
 De zorg voor de heuvels beschermt ons tegen overstromingen, zegt nieuw onderzoek
De zorg voor de heuvels beschermt ons tegen overstromingen, zegt nieuw onderzoek Hoe draagt biodiversiteit bij aan de duurzaamheid van een habitat?
Hoe draagt biodiversiteit bij aan de duurzaamheid van een habitat?  Klimaatmodellen met hoge resolutie presenteren alarmerende nieuwe projecties voor de VS
Klimaatmodellen met hoge resolutie presenteren alarmerende nieuwe projecties voor de VS Uit onderzoek blijkt dat de stijging van de zeespiegel en weersgerelateerde schokken ervoor zorgden dat het moeras van Louisiana afstierf
Uit onderzoek blijkt dat de stijging van de zeespiegel en weersgerelateerde schokken ervoor zorgden dat het moeras van Louisiana afstierf  Voorbij de oceanen:microplastics vervuilen rivieren en meren, te
Voorbij de oceanen:microplastics vervuilen rivieren en meren, te
Hoofdlijnen
- Wat is het belangrijkste doel van een celwand in plantencel?
- Wetten van aantrekking:bestuivers gebruiken meerdere signalen om bloemen op verschillende continenten te identificeren
- Hoe heet de wetenschap van zeer kleine planten en dieren?
- Tot welke phylum behoort paling?
- Hoe ziet een ribosomen eruit in plantencel?
- Lichaamsmassa van bijen, ziekteverwekkers en lokale klimaatinvloeden hittetolerantie
- Geavanceerde microscopen helpen wetenschappers begrijpen hoe cellen eiwitten afbreken
- Hoe de mitochondriën van een cel hun eigen eiwitfabrieken maken
- Waarom noemde de wetenschapper Silver Argentum?
- Wetenschappers maken de kleinste onderling verbonden kettingen ter wereld

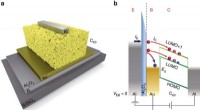
- Marcus-regime in organische apparaten - grensvlakladingsoverdrachtsmechanisme geverifieerd
- Kleverig als het nat is:sterke kleefstof voor wondgenezing
- Trek uw eigen elektroden om de ontwikkeling van microdetectieapparatuur te versnellen

- Na meer dan een decennium, ChIP-seq kan toch kwantitatief zijn
 Wat is de energietransformatie van een gloedstick?
Wat is de energietransformatie van een gloedstick?  Beveiligingspersoneel gaat dinsdag staken op luchthaven Frankfurt
Beveiligingspersoneel gaat dinsdag staken op luchthaven Frankfurt Ingenieurs ontwikkelen 'slimme brillen' die automatisch scherpstellen op wat de drager ziet
Ingenieurs ontwikkelen 'slimme brillen' die automatisch scherpstellen op wat de drager ziet  Hoe werkt ultrasoonapparaat?
Hoe werkt ultrasoonapparaat?  Welke planten moeten gezond groeien?
Welke planten moeten gezond groeien?  Webb onthult een sterrenstelsel dat schittert met de oudste sterrenhopen van het universum
Webb onthult een sterrenstelsel dat schittert met de oudste sterrenhopen van het universum  Samsung opent 's werelds grootste smartphonefabriek in India
Samsung opent 's werelds grootste smartphonefabriek in India Studie:Groene thee kan de manier waarop we smaak waarnemen veranderen
Studie:Groene thee kan de manier waarop we smaak waarnemen veranderen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

