
Wetenschap
Hoe is een natriumatoom met een massa -nummer 22 anders dan één 24?
* Massienummer: Het massagummer vertegenwoordigt het totale aantal protonen en neutronen in de kern van een atoom.
* protonen: Alle natriumatomen hebben 11 protonen. Dit is wat hen als natrium definieert.
* neutronen: Het verschil in massanummer komt van de neutronen.
* Een natriumatoom met een massa -nummer van 22 heeft 11 neutronen (22 - 11 =11).
* Een natriumatoom met een massa -nummer van 24 heeft 13 neutronen (24 - 11 =13).
Samenvattend:
* Beide atomen zijn natrium omdat ze 11 protonen hebben.
* Het atoom met een massaal aantal van 24 heeft twee extra neutronen in vergelijking met het atoom met een massa -nummer van 22.
Dit worden isotopen genoemd - Atomen van hetzelfde element met verschillende aantallen neutronen. Isotopen hebben dezelfde chemische eigenschappen maar enigszins verschillende fysische eigenschappen vanwege hun verschillende massa's.
 In twee moleculen van koolstofdioxide 2co2 zijn er hoeveel atomen en waar ze van hebben gemaakt?
In twee moleculen van koolstofdioxide 2co2 zijn er hoeveel atomen en waar ze van hebben gemaakt?  Welke warmtegasproductie en kleurverandering kunnen allemaal bewijs zijn van chemische verandering.
Welke warmtegasproductie en kleurverandering kunnen allemaal bewijs zijn van chemische verandering.  Waarom is kwik slecht in het delen van elektronen?
Waarom is kwik slecht in het delen van elektronen?  Is verfafbijtmiddel een zuur of een base?
Is verfafbijtmiddel een zuur of een base?  Waarom lost bariumhydroxide op in water, terwijl magnesium niet?
Waarom lost bariumhydroxide op in water, terwijl magnesium niet?
 Hoe beïnvloedt de opwarming van de aarde insecten?
Hoe beïnvloedt de opwarming van de aarde insecten?  Waarom we kin hebben:Onderzoekers beweren dat de kin voortkomt uit evolutie, en niet uit mechanische krachten
Waarom we kin hebben:Onderzoekers beweren dat de kin voortkomt uit evolutie, en niet uit mechanische krachten  Een nieuwe studie vindt onderzoekslacunes in milieuwetenschappelijke disciplines in het Noordpoolgebied
Een nieuwe studie vindt onderzoekslacunes in milieuwetenschappelijke disciplines in het Noordpoolgebied Niet-fotosynthetische vegetatie helpt de nauwkeurigheid van de beoordeling van de impact van winderosie te verbeteren
Niet-fotosynthetische vegetatie helpt de nauwkeurigheid van de beoordeling van de impact van winderosie te verbeteren  Nieuw onderzoek kraakt de code voor toekomstige exploratie van olie en gas in de Jizhong-depressie
Nieuw onderzoek kraakt de code voor toekomstige exploratie van olie en gas in de Jizhong-depressie
Hoofdlijnen
- Mariene wetenschappers bepalen hoe de larven van een veel voorkomende koraalsoort reageren op omgevingsstress
- Wat is het voordeel van aseksuele sporen?
- Student onderzoekt hoe de sms-cultuur is geëvolueerd
- Wat zijn de bacteriën die atherosclerose veroorzaken?
- Beschrijf de componenten van replicatiemachine.
- De genetische blauwdruk van woestijnpopulieren:inzichten in aanpassings- en overlevingsmechanismen
- Waarom moet een organisme een stabiele interne toestand behouden?
- In welke richting wordt voedsel overgedragen in een vasculaire plant?
- Welke structuur in een cel bestaat voornamelijk uit fosfolipide dubbellaag?
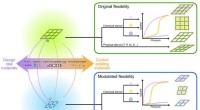
- Op weg naar het ontwerpen/beheersen van flexibiliteit van MOF's
- Palladium, ontmoet koper:onderzoekers gebruiken machine learning om katalysatoren te verbeteren

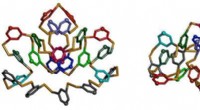
- Zelfgebouwde gevouwen macrocycles maken met lage symmetrie
- Gladde katheter met dubbele werking bestrijdt bacteriën
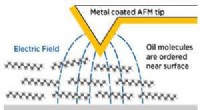
- Weer een stap dichter bij afstembare vloeistoffen
 Hoe helikopters werken
Hoe helikopters werken  Pinterest plant 2019 beursdebuut:rapport
Pinterest plant 2019 beursdebuut:rapport Wat zorgt ervoor dat dit invasieve, niet-inheemse rietgras gedijt in de wetlands?
Wat zorgt ervoor dat dit invasieve, niet-inheemse rietgras gedijt in de wetlands?  Aandeelhouders stemmen in met overname Takedas $ 60 miljard Shire
Aandeelhouders stemmen in met overname Takedas $ 60 miljard Shire School kan de sleutel zijn tot verbetering voor kinderen in de sociale zorg
School kan de sleutel zijn tot verbetering voor kinderen in de sociale zorg Wat wordt er gevormd als 2 glucosemoleculen worden gecombineerd?
Wat wordt er gevormd als 2 glucosemoleculen worden gecombineerd?  Hoe oefent een object zwaartekracht uit op elk ander object?
Hoe oefent een object zwaartekracht uit op elk ander object?  Wanneer zoutzuur en magnesiumcarbonaat reageren, wat produceren ze?
Wanneer zoutzuur en magnesiumcarbonaat reageren, wat produceren ze?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

