
Wetenschap
Wat veroorzaakt een neerslagreactie tussen twee oplosbare verbinding?
Hier is een uitsplitsing:
1. Oplosbare verbindingen:
* Deze verbindingen lossen op in water en vormen ionen. Wanneer bijvoorbeeld natriumchloride (NaCl) oplost in water, vormt dit natriumionen (Na+) en chloride-ionen (Cl-).
2. Vorming van een onoplosbaar product:
* Wanneer twee oplosbare verbindingen worden gemengd, kunnen hun ionen mogelijk combineren om een nieuwe verbinding te vormen.
* Als deze nieuwe verbinding onoplosbaar is In water blijft het niet opgelost en vormt in plaats daarvan een vast neerslag.
3. Drijvende kracht:
* De drijvende kracht achter neerslagreacties is de vorming van een stabieler product . Onoplosbare verbindingen zijn over het algemeen stabieler dan de originele ionen in oplossing.
Voorbeeld:
Overweeg de reactie tussen zilvernitraat (Agno3) en natriumchloride (NaCl):
* Agno3 (aq) + NaCl (aq) → Agcl (s) + nano3 (aq)
* Zilvernitraat en natriumchloride zijn beide oplosbaar, maar zilverchloride (AGCL) is onoplosbaar.
* Wanneer deze oplossingen worden gemengd, combineren zilverionen (Ag+) en chloride-ionen (Cl-) om het vaste zilveren chloride-neerslag te vormen.
Samenvattend treedt een neerslagreactie op wanneer de combinatie van ionen uit twee oplosbare verbindingen leidt tot de vorming van een onoplosbaar product, dat vervolgens uit oplossing neerslaat.
 Een mineraal met zijdeachtige glans die wordt gebruikt in babypoeder?
Een mineraal met zijdeachtige glans die wordt gebruikt in babypoeder?  Ionische verbindingen zoals natriumchloride NaCl lossen gemakkelijk op in water?
Ionische verbindingen zoals natriumchloride NaCl lossen gemakkelijk op in water?  Onderzoekers doen inspanningen om parasitaire rondwormen te bestrijden
Onderzoekers doen inspanningen om parasitaire rondwormen te bestrijden Video:Wat is er precies gebeurd in Tsjernobyl?
Video:Wat is er precies gebeurd in Tsjernobyl? Hoe de hoogste ionisatie-energie te bepalen
Hoe de hoogste ionisatie-energie te bepalen
Hoofdlijnen
- Wat is de wetenschappelijke verklaring voor seks bij mensen?
- Kan iemand een kort verhaal schrijven met behulp van de woorden mitochondria cytoplasma chloroplast en chlorofyl nucleolus kernweefsel organen vacuole chromosoom?
- Blueprint laat zien hoe planten een suikertransportbaan aanleggen
- Welke vorm van bacterie is tyfus?
- Hoe verdrijft een cel grote deeltjes?
- Hoeveel ATP-moleculen worden er gegenereerd voor één molecuul glucose?
- Hoe microplastics in de mariene atmosfeer terechtkomen
- Waarom leven vogels doorgaans langer dan zoogdieren?
- Hoe te differentiëren tussen mitose en cytokinese
- Onderzoekers combineren levende en levenloze stoffen

- Nieuw materiaal kan de productie van plastic energiezuiniger maken
- Carbon black gerecycled uit autobanden

- Onderzoekers maken binnenlandse hoogwaardige bipolaire membranen mogelijk

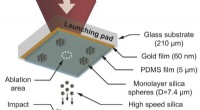
- Onderzoekers laten zien dat materialen vanzelf sterker worden wanneer ze met zeer hoge snelheid worden geraakt
 USA Today-uitgever getarget op buy-out
USA Today-uitgever getarget op buy-out Onderzoekers doen baanbrekende ontdekking in rekbare elektronische materialen
Onderzoekers doen baanbrekende ontdekking in rekbare elektronische materialen Hoeveel soorten eclips zijn er?
Hoeveel soorten eclips zijn er?  Waarom heeft een regenworm een open of gesloten bloedsomloop?
Waarom heeft een regenworm een open of gesloten bloedsomloop?  Hoe verandert het proces van fotosynthese gedurende een volledige dag?
Hoe verandert het proces van fotosynthese gedurende een volledige dag?  Crossly-vermenigvuldiging
Crossly-vermenigvuldiging Uit analyse van sportanalyse blijkt dat gedeeld succes in het verleden onder teamleden de kans op toekomstige overwinningen vergroot
Uit analyse van sportanalyse blijkt dat gedeeld succes in het verleden onder teamleden de kans op toekomstige overwinningen vergroot Wat is het sediment afgezet in waterlichamen en andere laaggelegen gebieden?
Wat is het sediment afgezet in waterlichamen en andere laaggelegen gebieden?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

