
Wetenschap
Waarom wordt calciumchloride bij roesttexperimenten soms gebruikt?
* vocht: Calciumchloride is een hygroscopische stof, wat betekent dat het gemakkelijk vocht uit de lucht absorbeert. Dit creëert een vochtige omgeving rond het metaal, wat cruciaal is voor roestvorming. Roest (ijzeroxide) wordt gevormd door een chemische reactie tussen ijzer, zuurstof en water.
* elektrolyt: Calciumchloride lost op in water en vormt een elektrolytoplossing. Deze oplossing leidt elektriciteit, waardoor de stroming van ionen mogelijk is die de elektrochemische reacties die betrokken zijn bij roesten verder versnellen.
* pH: Calciumchloride -oplossingen zijn enigszins zuur. Deze zuurgraad kan de oplossing van de beschermende oxidelaag op het metaaloppervlak verder bevorderen, waardoor het gevoeliger is voor roest.
Samenvattend: Door vocht, een elektrolyt en een enigszins zure omgeving te bieden, versnelt calciumchloride het roestproces, waardoor het gemakkelijker is om de effecten van roestvorming in experimenten te observeren en te bestuderen.
Opmerking: Het is belangrijk op te merken dat hoewel calciumchloride roestversnelt, dit niet de enige factor is. Andere factoren zoals het type metaal, temperatuur en blootstelling aan zuurstof spelen ook een rol.
 Wat is de netto ionische vergelijking voor magnesiumchloride en zilvernitraat?
Wat is de netto ionische vergelijking voor magnesiumchloride en zilvernitraat?  Eriochrome Black T Solution Preparation
Eriochrome Black T Solution Preparation  Het ontdekken van nieuwe medicijnen is een lang en duur proces:chemische verbindingen die screeningtools misleiden, maken het nog moeilijker
Het ontdekken van nieuwe medicijnen is een lang en duur proces:chemische verbindingen die screeningtools misleiden, maken het nog moeilijker Ingenieurs maken transistors en elektronische apparaten volledig van draad
Ingenieurs maken transistors en elektronische apparaten volledig van draad Zeven stappen in wetenschappelijk onderzoek en de betekenis ervan?
Zeven stappen in wetenschappelijk onderzoek en de betekenis ervan?
 Afvalwater bevat voedingsstoffen, energie en edele metalen - wetenschappers leren hoe ze deze kunnen terugwinnen
Afvalwater bevat voedingsstoffen, energie en edele metalen - wetenschappers leren hoe ze deze kunnen terugwinnen Maïsproductiviteit in realtime:Satellieten, veldcamera's, en boeren werken samen
Maïsproductiviteit in realtime:Satellieten, veldcamera's, en boeren werken samen Een kijkje in de biologische koolstofpomp van de oceanen
Een kijkje in de biologische koolstofpomp van de oceanen Een nieuwe kijk op de uitstoot van tropische bossen
Een nieuwe kijk op de uitstoot van tropische bossen Kan klimaatverandering een hele nieuwe categorie orkaan voortbrengen?
Kan klimaatverandering een hele nieuwe categorie orkaan voortbrengen?
Hoofdlijnen
- Beperkingen van enzymen gebruikt in Forensic Science
- Wat zijn abiotische en biotische factoren van een kelp -bos?
- De VS bevorderen de herziening van de lithiummijn in Nevada vanwege zorgen over bedreigde wilde bloemen
- Wilde bijen worden bedreigd door huisbijen, invasieve soorten, ziekteverwekkers en klimaatverandering, maar wij kunnen helpen
- Moderne mensen genereren meer hersenneuronen dan Neanderthalers
- Wetenschappers die biotechnologieën ontwikkelen, gebruiken vaak vectoren in hun onderzoek. Welke uitspraak beschrijft het beste wat een vector is?
- Wat is het effect van mutaties in levende organismen?
- Drie hoofdafdelingen van de hersenen?
- Wanneer twee soorten zo nauw samenwerken dat ze aan elkaar zijn aangepast, wordt de interactie genoemd?
- Wetenschappers ontwikkelen proces om brandstof van hogere kwaliteit te produceren uit bioafval

- schoner, sterker, harder:Nieuwe technologie verbetert duurzaam beton

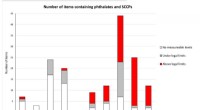
- Gifstoffen in oud speelgoed een obstakel voor circulaire economie
- Onderzoek naar stikstoffixatie kan licht werpen op biologisch mysterie

- Een nieuwe gids voor ontdekkingsreizigers van de submicroscopische wereld in ons

 Als je van links naar rechts over het spectrum gaat, wat gebeurt er frequentie en energie van golven?
Als je van links naar rechts over het spectrum gaat, wat gebeurt er frequentie en energie van golven?  Opladen door veranderingen in luchtvochtigheid
Opladen door veranderingen in luchtvochtigheid Onderzoekers creëren kader om cyberaanvallen op auto's met internetverbinding te stoppen
Onderzoekers creëren kader om cyberaanvallen op auto's met internetverbinding te stoppen Studie van wetten in materie en beweging?
Studie van wetten in materie en beweging?  Heeft Venus ooit oceanen gehad?
Heeft Venus ooit oceanen gehad? Archeologen ontdekken dat Neanderthalers en Homo sapiens woonruimtes op dezelfde manier organiseerden
Archeologen ontdekken dat Neanderthalers en Homo sapiens woonruimtes op dezelfde manier organiseerden  Hoeveel vierkante gevoel is 115 inch bij 2 voet?
Hoeveel vierkante gevoel is 115 inch bij 2 voet?  Video:Is er een snelle oplossing voor de verzuring van de oceanen?
Video:Is er een snelle oplossing voor de verzuring van de oceanen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

