
Wetenschap
Wat is de chloride -ionen en chlooratoomelektronenconfiguratie?
chlooratoom (CL)
* Atomisch nummer: 17, wat betekent dat het 17 protonen en 17 elektronen heeft.
* Elektronenconfiguratie: 1S² 2S² 2P⁶ 3S² 3P⁵
Verklaring:
* De elektronenconfiguratie volgt het AUFBAU -principe en de regel van HUW, en vult orbitalen in volgorde van toenemende energie.
* 1S²: Het eerste energieniveau (n =1) heeft twee elektronen in de 1s orbital.
* 2S²: Het tweede energieniveau (n =2) heeft twee elektronen in de 2s orbital.
* 2p⁶: Het tweede energieniveau heeft ook zes elektronen in de drie 2p -orbitalen.
* 3S²: Het derde energieniveau (n =3) heeft twee elektronen in de 3s orbital.
* 3P⁵: Het derde energieniveau heeft vijf elektronen in de drie 3p -orbitalen.
chloride -ion (Cl⁻)
* Formatie: Chloor krijgt één elektron om een stabiel octet (acht elektronen) in zijn buitenste schaal te bereiken.
* Elektronenconfiguratie: 1S² 2S² 2P⁶ 3S² 3P⁶
Verklaring:
* Het chloride -ion heeft nu 18 elektronen (17 origineel + 1 gewonnen).
* Het toegevoegde elektron vult het laatste 3p -orbitaal, waardoor het een volledige buitenste schaal krijgt.
Key Takeaway:
* Het chloride -ion is stabieler dan het chlooratoom omdat het een volledige buitenste schaal van elektronen heeft.
 Schuilplaats, veiligste luchtinlaatlocaties geïdentificeerd tijdens stedelijke vervuilingsgebeurtenissen
Schuilplaats, veiligste luchtinlaatlocaties geïdentificeerd tijdens stedelijke vervuilingsgebeurtenissen Wat is het tegenovergestelde van een verrekijker?
Wat is het tegenovergestelde van een verrekijker?  Welke dieren leven in het kustgebied?
Welke dieren leven in het kustgebied?  Natuurlijke algenpopulatie kan verklaren hoe veranderingen in het milieu de wereldwijde koolstofcycli beïnvloeden
Natuurlijke algenpopulatie kan verklaren hoe veranderingen in het milieu de wereldwijde koolstofcycli beïnvloeden Mysterieuze gigantische stofdeeltjes gevonden op zwaartekracht tartende afstanden
Mysterieuze gigantische stofdeeltjes gevonden op zwaartekracht tartende afstanden
Hoofdlijnen
- Zelfs wilde zoogdieren hebben regionale dialecten
- Wat is een organisme dat de hele of een andere roept doodt en eet?
- Wat betekent oxiatie?
- Waar werken en wonen wetenschappers?
- Kun je het woord microbiologie in een zin gebruiken?
- Wat zijn de oorzaken van zulke overeenkomsten en verschillen in genen?
- Hoe talin-eiwit de intercellulaire verbinding onderhoudt terwijl het kracht overbrengt
- Een flitsende gele keelzanger? Daar zijn genen voor
- Wat worden gevormde groepen cellen die samenwerken als organen in orgaansystemen?
- Power-to-gas-installatie met hoog rendement

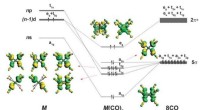
- Chemici tonen aan dat het 18-elektronenprincipe niet beperkt is tot overgangsmetalen
- Activering van prodrug met behulp van in eiwit omhulde goudkatalysator
- Diamant van nanoformaat zal materialen voor maritiem transport verbeteren

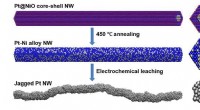
- Ruwe oppervlakken bieden extra locaties voor energieopwekkende reacties in brandstofcellen
 Hoeveel evenals zijn er op aarde?
Hoeveel evenals zijn er op aarde?  Playboy verlaat Facebook om privacyschandaal
Playboy verlaat Facebook om privacyschandaal Wetenschappers gebruiken katalysatoren om kankercellen van binnenuit te vernietigen
Wetenschappers gebruiken katalysatoren om kankercellen van binnenuit te vernietigen Wat zijn de rollen van tweede boodschappers in signaaltransductieroutes?
Wat zijn de rollen van tweede boodschappers in signaaltransductieroutes?  Repetitietijd voor NASA's asteroïde bemonsteringsruimtevaartuig
Repetitietijd voor NASA's asteroïde bemonsteringsruimtevaartuig Intens laserlicht wijzigt de elektronenparen
Intens laserlicht wijzigt de elektronenparen Hoe levende materialen uit algen het beste koolstof kunnen vastleggen
Hoe levende materialen uit algen het beste koolstof kunnen vastleggen  Hoe gedragen deeltjes zich in een oplossing?
Hoe gedragen deeltjes zich in een oplossing?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

