
Wetenschap
Wat is een hydrofobe verbinding?
Hier is een uitsplitsing:
* Hydrofoob: Betekent "water vrezen".
* Water: Een polair molecuul, wat betekent dat het een enigszins positief uiteinde en een enigszins negatief uiteinde heeft als gevolg van ongelijke delen van elektronen.
* Hydrofobe verbindingen: Zijn meestal niet -polair, wat betekent dat hun elektronen gelijkmatig zijn verdeeld, en ze missen de positieve en negatieve ladingen die hen naar water zouden trekken.
Denk er op deze manier aan: Olie en water mengen niet. Olie is een hydrofobe verbinding.
Voorbeelden van hydrofobe verbindingen:
* vetten en oliën: Ze bestaan uit lange ketens van koolstof- en waterstofatomen.
* wassen: Vergelijkbaar met vetten, maar met langere ketens.
* Bepaalde eiwitten: Sommige eiwitten hebben regio's die hydrofoob zijn, waardoor ze in specifieke vormen worden opgevouwen.
* gassen: De meeste gassen zijn niet -polair en daarom hydrofoob.
Belangrijke opmerking:
Hoewel hydrofobe verbindingen niet oplossen in water, kunnen ze nog steeds in water worden verspreid als kleine druppeltjes (zoals olie in een vinaigrette). Dit wordt een emulsie genoemd .
Waarom is hydrofobiciteit belangrijk?
Hydrofobiciteit speelt een cruciale rol in veel biologische processen, zoals:
* Celmembraanstructuur: Celmembranen hebben een hydrofoob interieur, dat hen helpt te reguleren wat de cel binnenkomt en verlaat.
* Eiwitvouwen: Hydrofobe interacties helpen eiwitten in hun juiste vormen te vouwen.
* Waterdichte: Was en vetten maken oppervlakken waterdicht, zoals veren en bladeren.
Hoofdlijnen
- Wat zijn de elementen van nucleic
- Het verschil tussen hoe interne en externe regulatoren werken
- Hoe de worm weet waar zijn neus is
- Wat is de meest geaccepteerde definitie voor een soort over biologie?
- Welke functie hebben co-enzymen bij de ademhaling?
- Wat is de wetenschappelijke naam voor Diplococcus Pheumoniae?
- Wat bepaalt welke eigenschappen het meest frequent aan de volgende generatie worden doorgegeven?
- Waarom eten zeevogels plastic? Het antwoord stinkt
- Begrijpt jouw hond het als je zegt ‘haal de bal’? Een nieuwe studie in Hongarije zegt van wel
- Efficiënte perovskiet fotovoltaïsche energie optimaliseren

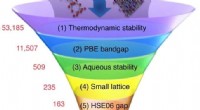
- Uitgebreide elektronische structuurmethoden voor materiaalontwerp
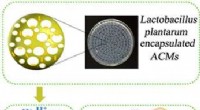
- Probiotica beschermen tegen de maag
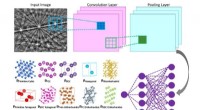
- Machine learning-techniek versnelt de bepaling van de kristalstructuur
- Video:vijf dingen die je misschien niet wilt combineren met anticonceptie

 Hoogwaardige natriumionbatterijen die kopersulfide gebruiken
Hoogwaardige natriumionbatterijen die kopersulfide gebruiken Wie was de tweede persoon die Moon bereikte?
Wie was de tweede persoon die Moon bereikte?  Waarom oer-asteroïden die enorme botsingen hebben vermeden, allemaal ongeveer even groot lijken te zijn?
Waarom oer-asteroïden die enorme botsingen hebben vermeden, allemaal ongeveer even groot lijken te zijn? Hubble detecteert beschermend schild dat een paar dwergstelsels verdedigt
Hubble detecteert beschermend schild dat een paar dwergstelsels verdedigt Hoe wordt zuurstof vervangen?
Hoe wordt zuurstof vervangen?  Onderzoekers vragen Amerikanen:'Hoe ziet God eruit?'
Onderzoekers vragen Amerikanen:'Hoe ziet God eruit?'  Een hoeveelheid ideaal gas is 0 graden Celsius nog een keer zo heet wat de temperatuur?
Een hoeveelheid ideaal gas is 0 graden Celsius nog een keer zo heet wat de temperatuur?  Wat is het effect van temperatuur op toestanden van materie?
Wat is het effect van temperatuur op toestanden van materie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


