
Wetenschap
Welke halfreactie vindt plaats bij de kathode van een galvanische cel met koper- en zilverelektroden?
1. Identificeer het meer positieve reductiepotentieel:
* Zoek de standaardreductiepotentialen op voor koper en zilver:
* Cu²⁺ (aq) + 2e⁻ → cu (s) e ° =+0.34 v
* Ag⁺ (aq) + e⁻ → Ag (s) e ° =+0,80 V
* Hoe hoger het reductiepotentieel, hoe groter de kans dat de soort moet worden verminderd. Zilver heeft een hoger reductiepotentieel dan koper, wat aangeeft dat het gemakkelijker wordt verminderd.
2. Bepaal de kathode:
* De kathode is waar reductie optreedt (winst van elektronen). Omdat zilver het hogere reductiepotentieel heeft, zal het worden verminderd in de kathode.
3. Schrijf de halfreactie:
* De halfreactie bij de kathode is de vermindering van zilverionen:
Ag⁺ (aq) + e⁻ → Ag (s)
Samenvatting:
In een galvanische cel met koper- en zilverelektroden is de halfreactie bij de kathode de reductie van zilverionen tot vast zilver.
 Oude veranderingen langs de Hudson bieden een glimp van hoe ijskappen groeiden
Oude veranderingen langs de Hudson bieden een glimp van hoe ijskappen groeiden Studie:Klimaatverandering treft kinderen onevenredig
Studie:Klimaatverandering treft kinderen onevenredig Oost-Australië heeft honderden raadselachtige vulkanen. Nieuw onderzoek laat zien hoe ze zijn ontstaan
Oost-Australië heeft honderden raadselachtige vulkanen. Nieuw onderzoek laat zien hoe ze zijn ontstaan Hoe ID Mountain Lion Poop
Hoe ID Mountain Lion Poop  Akoestische beeldvorming onthult verborgen kenmerken van megathrust-fout voor Costa Rica
Akoestische beeldvorming onthult verborgen kenmerken van megathrust-fout voor Costa Rica
Hoofdlijnen
- Wat voor soort twee materialen gebruikt het blad om suiker te produceren?
- Hoe de embryonale cellen van een worm zijn ontwikkelingspotentieel veranderen
- Mensen zijn geëvolueerd met hun microbioom. Net als genen gaan je darmmicroben van de ene generatie naar de volgende
- De Durian-industrie zou kunnen lijden zonder de bedreigde fruitvleermuis
- Waarom gebruikte Mendel erwtenplanten in zijn experimenten?
- Wat is alumanodi?
- Wat is een groter molecuul of virus?
- Welke van de volgende beschrijft de functies van de longen?
- Wat is het voordeel van het feit dat het DNA goed is ingepakt in de chromosomen?
- Eenvoudig apparaat bewaakt de gezondheid met behulp van zweet

- Onderzoek naar levensvatbare, veilige batterijen overwinnen hoge weerstand, halfgeleiderbarrières met lage capaciteit

- Onderzoekers ontwikkelen materialen om geneesmiddelen uit afvalwater te verwijderen
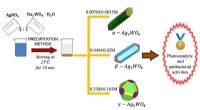
- Meer realistische en nauwkeurige organen-op-chips
- Ons water reinigen met baanbrekende bio-geïnspireerde chemie
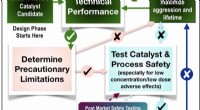
 Politie zegt dat hacker ID heeft verborgen bij inbreuk op privacy in Australië
Politie zegt dat hacker ID heeft verborgen bij inbreuk op privacy in Australië Bats:Wat goed klinkt, smaakt niet altijd
Bats:Wat goed klinkt, smaakt niet altijd  Wat is het verschil tussen een oplossing en een mengsel?
Wat is het verschil tussen een oplossing en een mengsel?  Studie vindt de kosten van partijdigheid onder federale arbeiders
Studie vindt de kosten van partijdigheid onder federale arbeiders Welke metalen kunnen oxyacetyleen lassen?
Welke metalen kunnen oxyacetyleen lassen?  Waarom is het minder waarschijnlijk dat rijke consumenten luxeartikelen kopen tijdens een recessie?
Waarom is het minder waarschijnlijk dat rijke consumenten luxeartikelen kopen tijdens een recessie?  Waaruit bestaat natriumcarbonaat?
Waaruit bestaat natriumcarbonaat?  Cool Earth-theorie werpt meer licht op diamanten
Cool Earth-theorie werpt meer licht op diamanten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

