
Wetenschap
De pH van een oplossing A is 2 B 4 Hoe verhoudt de concentratie waterstofionen zich?
* pH- en waterstofionconcentratie: PH is een maat voor de zuurgraad of alkaliteit van een oplossing. Het is gebaseerd op de concentratie van waterstofionen (H+). Een lagere pH geeft een hogere concentratie waterstofionen aan, wat betekent dat de oplossing zuurder is.
* Vergelijking van oplossingen A en B:
* Oplossing A heeft een pH van 2.
* Oplossing B heeft een pH van 4.
Omdat oplossing A een lagere pH heeft dan oplossing B, heeft het een hogere concentratie waterstofionen .
specifiek:
* Een verschil van 2 pH -eenheden betekent dat de concentratie waterstofionen in oplossing A 100 keer groter is dan in oplossing B. Dit komt omdat de pH -schaal logaritmisch is.
Hoofdlijnen
- Wat verdeelt zich tijdens cytokinese bij een vrouw ongelijk?
- Welke twee mensen worden gecrediteerd voor het ontdekken van de vorm van DNA?
- Een bedieningsknop voor vet? Eiwit dat andere eiwitten maakt, reguleert ook het vetgehalte
- Bacteriën die geen aerobe ademhaling vereisen?
- Twee menselijke eiwitten blijken van invloed te zijn op de manier waarop het 'springende gen' zich verspreidt
- Welke term zou worden toegepast op een regulerende toestand die optreedt wanneer eiwitten de transcriptie geassocieerd met een bepaald deel van DNA aanzienlijk vermindert?
- Hoe werken het ademhalingsstelsel en het cardiovasculaire systeem samen?
- Europese mollen kunnen in de winter met een tiende krimpen om energie te besparen
- Hoe kan biotechnologie de opwarming van de aarde stoppen?
- Video:Waarom limoensap je huid verbrandt in de zon

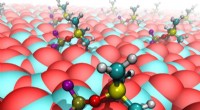
- Wetenschappers kunnen katalysatoren met één atoom voorspellen en ontwerpen voor belangrijke chemische reacties

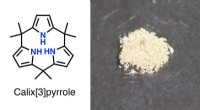
- Pyrroolchemie:goede dingen komen in drieën
- De wetenschap achter ingelegde elektrolyten in batterijen
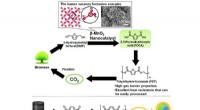
- Groene katalysatoren met aardrijke metalen versnellen de productie van biobased plastic
 Nieuw thermo-elektrisch materiaal levert recordprestaties
Nieuw thermo-elektrisch materiaal levert recordprestaties In Zweden, wrak zou zusterschip kunnen zijn van iconisch schip
In Zweden, wrak zou zusterschip kunnen zijn van iconisch schip Luchtcirculatie beïnvloedt vorst meer dan opwarming van de aarde - voorlopig
Luchtcirculatie beïnvloedt vorst meer dan opwarming van de aarde - voorlopig Overstromingen bij mooi weer nemen toe naarmate de zeespiegel stijgt, NOAA zegt
Overstromingen bij mooi weer nemen toe naarmate de zeespiegel stijgt, NOAA zegt Wat maakt uranium?
Wat maakt uranium?  Meer mannen, meer problemen? Niet noodzakelijkerwijs, blijkt uit onderzoek
Meer mannen, meer problemen? Niet noodzakelijkerwijs, blijkt uit onderzoek  Wat is de dubbele helix?
Wat is de dubbele helix?  Verontreiniging met landbouwinsecticiden bedreigt de integriteit van het Amerikaanse oppervlaktewater op nationale schaal
Verontreiniging met landbouwinsecticiden bedreigt de integriteit van het Amerikaanse oppervlaktewater op nationale schaal
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


