
Wetenschap
Voordelen van oxidatie en vermindering van het leven?
Energieproductie:
* Cellulaire ademhaling: De meest cruciale rol van redoxreacties is in cellulaire ademhaling, waarbij glucose wordt afgebroken om energie te genereren (ATP). Oxidatie van glucose omvat het verwijderen van elektronen, en deze elektronen worden vervolgens gebruikt om zuurstof te verminderen, waardoor water ontstaat en energie loslaat. Deze energie voedt alle levensprocessen.
* fotosynthese: Planten gebruiken redoxreacties in fotosynthese om lichte energie vast te leggen en om te zetten in chemische energie in de vorm van glucose. Water wordt geoxideerd, waardoor elektronen worden vrijgelaten die worden gebruikt om koolstofdioxide te verminderen, waardoor glucose wordt gevormd.
Complexe moleculen bouwen:
* Biosynthese: Redox -reacties zijn essentieel voor het bouwen van complexe biomoleculen zoals eiwitten, vetten en koolhydraten. Deze processen omvatten het verminderen van kleinere moleculen door elektronen toe te voegen, waardoor grotere en complexere structuren worden gevormd.
* Metabole paden: Redox -reacties zijn betrokken bij tal van metabole routes, waaronder de synthese van aminozuren, nucleotiden en hormonen.
Andere belangrijke functies:
* Signaaltransductie: Redox -reacties spelen een rol in cellulaire signaalroutes, waar veranderingen in oxidatietoestanden specifieke reacties kunnen activeren.
* Defensiemechanismen: Sommige organismen gebruiken redoxreacties om toxines of reactieve zuurstofsoorten te produceren als afweermechanismen tegen pathogenen.
* Nutrient Absorptie: Redox -reacties zijn betrokken bij de opname van voedingsstoffen uit het milieu, waardoor organismen essentiële elementen kunnen verkrijgen voor groei en ontwikkeling.
Voorbeelden:
* brandende brandstof: Verbranding, het verbranden van brandstoffen zoals hout of benzine, is een redoxreactie die energie vrijgeeft door de oxidatie van de brandstof.
* roesten: Roest van ijzer is een ander voorbeeld van oxidatie, waarbij ijzeratomen elektronen verliezen en reageren met zuurstof, waardoor ijzeroxide (roest) wordt gevormd.
Conclusie:
Oxidatie en reductie zijn essentieel voor het leven, het stimuleren van energieproductie, biosynthese en tal van andere vitale functies. Het zijn fundamentele chemische reacties die ten grondslag liggen aan alle biologische processen, waardoor organismen kunnen gedijen en het leven kunnen behouden.
 Hoeveel chemische veranderingen of stappen zijn er alleen nodig om glucosemolecuul in twee pyruvinezuurmoleculen te splitsen?
Hoeveel chemische veranderingen of stappen zijn er alleen nodig om glucosemolecuul in twee pyruvinezuurmoleculen te splitsen?  Kan sublimatie worden gebruikt om een stof te identificeren?
Kan sublimatie worden gebruikt om een stof te identificeren?  Nieuwe strategie zorgt voor efficiënte en stabiele elektrolyse van kooldioxide in elektrolysecel voor vaste oxiden
Nieuwe strategie zorgt voor efficiënte en stabiele elektrolyse van kooldioxide in elektrolysecel voor vaste oxiden Directe transformatie van CH3Cl naar azijnzuur via een carbonyleringsreactie
Directe transformatie van CH3Cl naar azijnzuur via een carbonyleringsreactie  Wat worden chemicaliën die worden gebruikt om territoriale grenzen te markeren?
Wat worden chemicaliën die worden gebruikt om territoriale grenzen te markeren?
 Wetenschappers gebruiken satellieten om essentiële ondergrondse watervoorraden te meten
Wetenschappers gebruiken satellieten om essentiële ondergrondse watervoorraden te meten Onhoorbaar infrageluid ook nuttig voor weers- en klimaatvoorspellingen
Onhoorbaar infrageluid ook nuttig voor weers- en klimaatvoorspellingen Hoe de koffie-industrie op het punt staat te worden gebrand door klimaatverandering
Hoe de koffie-industrie op het punt staat te worden gebrand door klimaatverandering De sterkte van tektonische platen kan de vorm van het Tibetaanse plateau verklaren, studie vondsten
De sterkte van tektonische platen kan de vorm van het Tibetaanse plateau verklaren, studie vondsten Golfstroom wervelt als bron van ijzer
Golfstroom wervelt als bron van ijzer
Hoofdlijnen
- Waarom de harde Sneeuwbalaarde onze vroegste meercellige voorouders op gang bracht
- Wat is zymotechnologie?
- Genetici tonen aan dat COPIA-R7-transposon de immuniteit van zijn gastheer tegen pathogene micro-organismen verbetert
- Wat voor soort stimulus reist van het motorneuron naar skeletspier?
- Waarom is bioinformatica belangrijk in genetisch onderzoek?
- Mutualisme (biologie): definitie, types, feiten en voorbeelden
- Kunnen darmbacteriën die ons helpen bij het verteren van bier en brood ook ziektes bestrijden?
- Hoe kunnen kinderen van dezelfde ouders er zo verschillend uitzien?
- Zou je het noemen wanneer organismen concurreren om biotische en abiotische factoren van een ecosysteem?
- Rekbare natrium-ion batterij-elektroden gemaakt van suikerklontjes
- Een chip gebruiken om betere kankerbestrijdende medicijnen te vinden

- Hoe efficiënte organische zonnecellen te bouwen?

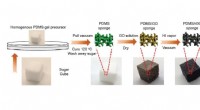
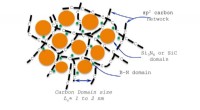
- Ingenieur patenteert waterachtig polymeer om keramiek op hoge temperatuur te maken
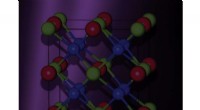
- Nieuwe katalysatoren maken van unieke metaallegeringen
 Maatschappelijk werkers proberen nieuwe manieren om tieners veilig te houden
Maatschappelijk werkers proberen nieuwe manieren om tieners veilig te houden Schimmelexperiment om te starten als Artemis I payload
Schimmelexperiment om te starten als Artemis I payload Polarstern-expeditie onderzoekt enorme gekalfde ijsberg
Polarstern-expeditie onderzoekt enorme gekalfde ijsberg Haargel zuur alkalisch of neutraal?
Haargel zuur alkalisch of neutraal?  Platentektoniek is mogelijk al vanaf het begin actief op aarde
Platentektoniek is mogelijk al vanaf het begin actief op aarde Wat zijn absolute zoutconcentraties?
Wat zijn absolute zoutconcentraties?  Observatorium ter grootte van een melkwegstelsel ziet mogelijke hints van zwaartekrachtgolven
Observatorium ter grootte van een melkwegstelsel ziet mogelijke hints van zwaartekrachtgolven Zeldzame trofische eieren achter het succes van slangenkopvissen?
Zeldzame trofische eieren achter het succes van slangenkopvissen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

