
Wetenschap
Wat zijn feiten over mangaan?
1. Symbool:Mn
Atoomnummer:25
Atoomgewicht:54,938045
Smeltpunt:1246 °C (2275 °F)
Kookpunt:2.066 °C (3.747 °F)
Dichtheid:7,21 g/cm³ (bij 20 °C)
2. Ontdekking:**
Mangaan werd voor het eerst geïsoleerd in 1774 door de Zweedse chemicus Johan Gottlieb Gahn.
3. Overvloed:
Mangaan is het twaalfde meest voorkomende element in de aardkorst, met een gemiddelde concentratie van ongeveer 1.000 ppm.
4. Kleur:
Mangaan is een hard, bros, zilverwit metaal met een roze tint.
5. Reactiviteit:
Mangaan is reactief en vormt gemakkelijk legeringen met andere metalen, zoals ijzer, koper en aluminium.
6. Oxidatietoestanden:
Mangaan vertoont een breed scala aan oxidatietoestanden, van -3 tot +7, waarbij +2 en +4 de meest voorkomende zijn.
7. Mineralen:
Mangaan wordt voornamelijk gewonnen uit mangaanertsen, zoals pyrolusiet (MnO2) en manganiet (MnOOH).
8. Belangrijkste toepassingen:**
Mangaan wordt voornamelijk gebruikt bij de productie van staal, waar het fungeert als legeringsmiddel om de sterkte en hardheid te vergroten. Het wordt ook gebruikt bij de vervaardiging van drogecelbatterijen, glas, keramiek en meststoffen.
9. Biologische rol:**
Mangaan is een essentieel sporenmineraal voor mens en dier. Het speelt een belangrijke rol bij botvorming, metabolisme en antioxiderende afweersystemen.
10. Gezondheidseffecten:**
Mangaan is over het algemeen veilig bij lage niveaus, maar hoge niveaus van blootstelling aan mangaanstof of -dampen kunnen een neurologische aandoening veroorzaken die manganisme wordt genoemd en die kan leiden tot trillingen, spierstijfheid en cognitieve stoornissen.
11. Milieu-impact:**
Door de winning en verwerking van mangaan kan mangaan in het milieu terechtkomen, waardoor de bodem, het water en de planten mogelijk worden verontreinigd. Hoge mangaangehalten in het milieu kunnen giftig zijn voor in het water levende organismen en kunnen ook risico's voor de menselijke gezondheid met zich meebrengen.
 Robotachtige zachte materie buigt, draait en kruipt wanneer geraakt met licht
Robotachtige zachte materie buigt, draait en kruipt wanneer geraakt met licht Bamboe inspireert tot een optimaal ontwerp voor lichtheid en taaiheid
Bamboe inspireert tot een optimaal ontwerp voor lichtheid en taaiheid Proces voor het maken van plastic flessen
Proces voor het maken van plastic flessen De rol van vastestofchemie bij de ontwikkeling van metaal-ionbatterijen
De rol van vastestofchemie bij de ontwikkeling van metaal-ionbatterijen Lachgas:waarom het milieu niet blij is met lachgas
Lachgas:waarom het milieu niet blij is met lachgas
 Uit onderzoek blijkt dat zwarte en Latijns-Amerikaanse Amerikanen onevenredig worden blootgesteld aan grotere temperatuurschommelingen
Uit onderzoek blijkt dat zwarte en Latijns-Amerikaanse Amerikanen onevenredig worden blootgesteld aan grotere temperatuurschommelingen  Ruimte is de sleutel tot monitoring van de verzuring van de oceaan
Ruimte is de sleutel tot monitoring van de verzuring van de oceaan Antarctische zee-ijsmodellen verbeteren voor het volgende IPCC-rapport
Antarctische zee-ijsmodellen verbeteren voor het volgende IPCC-rapport NASA's Aqua Satellite kijkt naar tropische cycloon Oma in de buurt van Vanuatu
NASA's Aqua Satellite kijkt naar tropische cycloon Oma in de buurt van Vanuatu Heeft er ooit leven bestaan op Mars? NASA's Perseverance-rover vindt organisch materiaal in gesteentemonsters
Heeft er ooit leven bestaan op Mars? NASA's Perseverance-rover vindt organisch materiaal in gesteentemonsters
Hoofdlijnen
- Noem 2 dingen die de bloeddruppelcellen gebruiken om te leven?
- Welke oorzaken smeren bij elektroforese?
- Zullen we weten of TRAPPIST-1e leven heeft?
- Knoei niet met de meiose:onderzoek wijst uit hoe reproductieve gezondheid de algehele gezondheid en het ouder worden beïnvloedt
- Wie controleert wie:Algen of zeeanemoon?
- Worden cellen geproduceerd uit niet-levende materialen?
- Hoe Cytoplasma voor een celproject te maken
- Soorten monomeren
- Hoe helpen centriolen de cel?
- Identificatie van het enzym dat betrokken is bij stressmanagement in bacteriën
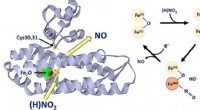
- Heterogene ethyleenhydroformylering maakt een zeer efficiënte industriële productie van propanal/n-propanol mogelijk

- Wetenschappers ontdekken nieuwe kankerbestrijdende molecule
- Video:De enige detox die je ooit nodig zult hebben

- Nieuwe vlinder-geïnspireerde waterstofsensor wordt aangedreven door licht

 Team ontwikkelt nieuw type antistollingsmiddel waarvan de werking snel kan worden gestopt
Team ontwikkelt nieuw type antistollingsmiddel waarvan de werking snel kan worden gestopt  Een verhaal over twee soorten vulkanen
Een verhaal over twee soorten vulkanen Gouden nanosondes die worden gebruikt om de bloedstroom in kleine bloedvaten te volgen
Gouden nanosondes die worden gebruikt om de bloedstroom in kleine bloedvaten te volgen VRKitchen:een interactieve virtuele omgeving om AI-agenten te trainen en te testen
VRKitchen:een interactieve virtuele omgeving om AI-agenten te trainen en te testen Afbeelding:DLR's Rollin Justin robot
Afbeelding:DLR's Rollin Justin robot Materiaal maken en aanpassen op atomaire schaal
Materiaal maken en aanpassen op atomaire schaal Bangladesh plant miljoen bomen om bliksemtol te verminderen
Bangladesh plant miljoen bomen om bliksemtol te verminderen Wat zijn de belangrijkste toepassingen van warmte-energie in de fysische wetenschap?
Wat zijn de belangrijkste toepassingen van warmte-energie in de fysische wetenschap?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

