
Wetenschap
Hoe is water een vloeistof?
Deze waterstofbinding creëert een sterke aantrekkingskracht tussen watermoleculen, die ze bij elkaar houdt en verhindert dat ze vrij langs elkaar kunnen bewegen. Als gevolg hiervan heeft water een relatief hoog kookpunt en een laag vriespunt in vergelijking met andere stoffen met een vergelijkbaar molecuulgewicht. Bij kamertemperatuur zijn deze waterstofbruggen nog steeds sterk genoeg om de watermoleculen in vloeibare toestand bij elkaar te houden.
De unieke eigenschappen van water, waaronder de oppervlaktespanning, cohesie en hoge specifieke warmtecapaciteit, worden ook beïnvloed door waterstofbruggen. Deze eigenschappen zijn essentieel voor het voortbestaan van veel organismen en spelen een cruciale rol in verschillende biologische processen.
 Onderzoekers tonen aan dat fruitvliegjes latente bioluminescentie hebben
Onderzoekers tonen aan dat fruitvliegjes latente bioluminescentie hebben  Team levert 's werelds eerste biosensorchips op basis van koper en grafeenoxide
Team levert 's werelds eerste biosensorchips op basis van koper en grafeenoxide De atomen in een watermolecuul worden bij elkaar gehouden door covalente bindingen. Dit betekent dat de gebonden atomen?
De atomen in een watermolecuul worden bij elkaar gehouden door covalente bindingen. Dit betekent dat de gebonden atomen?  Het element fluor heeft 9 elektronen. Wat is de elektronenconfiguratie voor een fluoratoom?
Het element fluor heeft 9 elektronen. Wat is de elektronenconfiguratie voor een fluoratoom?  Is chloortrifluoride een ionische verbinding of een moleculaire verbinding?
Is chloortrifluoride een ionische verbinding of een moleculaire verbinding?
 Onderzoekers modelleren regionale effecten van specifieke antropogene activiteiten, hun invloed op extreem brandweerrisico
Onderzoekers modelleren regionale effecten van specifieke antropogene activiteiten, hun invloed op extreem brandweerrisico Hoe gemanipuleerde bacteriën olie-zandvervuiling en mijnafval kunnen opruimen?
Hoe gemanipuleerde bacteriën olie-zandvervuiling en mijnafval kunnen opruimen? Studie onthult wereldwijde rimpeleffecten van regionale waterschaarste
Studie onthult wereldwijde rimpeleffecten van regionale waterschaarste Tarwe en bankgras kunnen giftige metalen uit verontreinigde grond halen
Tarwe en bankgras kunnen giftige metalen uit verontreinigde grond halen Californië heeft steenkool gedumpt - is gas de volgende?
Californië heeft steenkool gedumpt - is gas de volgende?
Hoofdlijnen
- Wat zijn de zes menselijke levensprocessen?
- Hoe verschilt mitose in de cellen van dieren en planten?
- Native Plants & Animals of France
- DNA-modellen van paperclips maken
- Was de vroege evolutie van dieren coöperatief?
- Waarom gebaren we?
- Wat zijn de functies van de linker en rechter Atria?
- Eukaryotische cel: definitie, structuur en functie (met analogie en diagram)
- Zal klimaatverandering het risico op aflatoxine in Amerikaanse maïs vergroten?
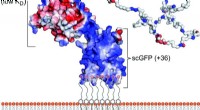
- Kunstmatige membraanbindende eiwitten om stamcellen naar het myocardium te leiden
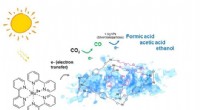
- Nieuwe door licht geactiveerde katalysator grijpt CO2 om ingrediënten voor brandstof te maken
- Moleculaire trillingen verminderen de maximaal haalbare fotospanning in organische zonnecellen
- Een nieuwe fluorescerende sonde die B-cellen van T-cellen kan onderscheiden

- Wetenschappers verbeteren de analyse van röntgengegevens met kunstmatige intelligentie

 Dodelijke hittegolven bedreigen de noordelijke graanschuur van China
Dodelijke hittegolven bedreigen de noordelijke graanschuur van China Afbeelding:Portugal brandwonden littekens
Afbeelding:Portugal brandwonden littekens Wat veroorzaakt een lager vriespunt?
Wat veroorzaakt een lager vriespunt?  Verkopers op websites met rubrieksadvertenties geven de voorkeur aan kopers uit welvarende buurten
Verkopers op websites met rubrieksadvertenties geven de voorkeur aan kopers uit welvarende buurten Onderzoekers bepalen hoe groepen beslissingen nemen
Onderzoekers bepalen hoe groepen beslissingen nemen  Beslissen over een aankoop:maakt het uit of u tijdens het winkelen naar boven of naar beneden kijkt?
Beslissen over een aankoop:maakt het uit of u tijdens het winkelen naar boven of naar beneden kijkt?  Hoeveel Orbeez kost het om een badkuip te vullen?
Hoeveel Orbeez kost het om een badkuip te vullen? Hoe evolueert het leven?
Hoe evolueert het leven?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

