
Wetenschap
Schrijf de verwachte elektronenconfiguratie in de grondtoestand voor overgangsmetaal op de eerste rij met de meeste ongepaarde elektronen?
Voor een overgangsmetaal op de eerste rij is de verwachte elektronenconfiguratie in de grondtoestand met de meest ongepaarde elektronen 3d ^ 5. Deze configuratie komt overeen met het metaalion met de hoogste oxidatietoestand, die doorgaans +5 is. De 3d^5-configuratie heeft vijf ongepaarde elektronen, wat aanleiding geeft tot het maximaal mogelijke paramagnetisme. De elektronenconfiguratie kan worden weergegeven als:
$$(1s)^2(2s)^2(2p)^6(3s)^2(3p)^6(3d)^5$$
Een voorbeeld van een overgangsmetaal op de eerste rij dat de 3d ^ 5-configuratie vertoont, is mangaan (Mn). In zijn +5 oxidatietoestand heeft mangaan de elektronenconfiguratie 1s^22s^22p^63s^23p^63d^5. Deze configuratie resulteert in vijf ongepaarde elektronen in de 3D-orbitalen, waardoor Mn5+ een van de meest paramagnetische ionen onder de overgangsmetalen op de eerste rij is.
Hoofdlijnen
- Wat zijn endorfines?
- Nieuw onderzoek laat zien hoe verstoring van de tarwehandel de voedselzekerheid kan beïnvloeden
- Wat is apoptose?
- In een warmere wereld is de helft van alle soorten in beweging. Waar gaan ze heen?
- Wanneer treedt acidose op?
- Het weer in november is een lastige tijd voor schildpadden
- Langzaam bevroren mensen? Recent onderzoek ondersteunt de mogelijkheid van cryopreservatie
- Wat zijn de 3 belangrijkste soorten RNA?
- Knoflook kan chronische infecties bestrijden
- Een nieuw textielmateriaal dat zichzelf kiemvrij houdt

- NIST pH-standaardreferentiematerialen ondersteunen een van de meest gemeten eigenschappen van de productie

- Door bacteriële enzymen te kopiëren, lab leert snel nieuwe klasse antibiotica moleculen schoon te synthetiseren, efficiënt

- Een nieuwe gerichte evolutietechniek om het potentieel van xeno-nucleïnezuren te ontsluiten
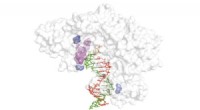
- Opruimen met cellulose
 Is een polygraaf een betrouwbare leugendetector?
Is een polygraaf een betrouwbare leugendetector? Oorlogsenquête:83% van de Israëlische NGO's is getroffen, gemengde reacties op overheidssteun, toename van buitenlandse steun
Oorlogsenquête:83% van de Israëlische NGO's is getroffen, gemengde reacties op overheidssteun, toename van buitenlandse steun  Onderzoek naar metaalafzetting in organen na gewrichtsvervanging
Onderzoek naar metaalafzetting in organen na gewrichtsvervanging Hoe menselijke urine de bodemgezondheid en waterkwaliteit kan verstoren
Hoe menselijke urine de bodemgezondheid en waterkwaliteit kan verstoren  NASA's volgen de grote orkaan Douglas in Hawaï
NASA's volgen de grote orkaan Douglas in Hawaï Ion-selectieve slimme poreuze membranen
Ion-selectieve slimme poreuze membranen Kronkelende randen kunnen grafeen versterken
Kronkelende randen kunnen grafeen versterken Nieuwe methode voor synthese van moleculaire waterstof stelt maatstaf voor platinavrije elektrokatalysatoren
Nieuwe methode voor synthese van moleculaire waterstof stelt maatstaf voor platinavrije elektrokatalysatoren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


