
Wetenschap
Wat zou er gebeuren als een atoom meer protonen dan elektronen zou hebben?
1. Positieve lading: Als een atoom meer protonen dan elektronen heeft, zou het een netto positieve lading hebben. Dit komt omdat protonen een positieve lading dragen, terwijl elektronen een negatieve lading dragen.
2. Elektrische aantrekkingskracht: De positieve protonen zouden de negatieve elektronen aantrekken, waardoor een sterke elektrische kracht in het atoom ontstaat.
3. Onstabiele configuratie: De onbalans tussen protonen en elektronen maakt het atoom instabiel. De sterke elektrostatische aantrekkingskracht tussen de protonen en de weinige elektronen zou ervoor zorgen dat het atoom veranderingen ondergaat om stabiliteit te bereiken.
4. Elektronenvangst: Om een stabielere toestand te bereiken, zou het atoom elektronen uit zijn omgeving kunnen opvangen. Dit proces wordt elektronenvangst genoemd en resulteert in de vermindering van het aantal protonen in de kern.
5. Bètaverval: Een ander mogelijk mechanisme om stabiliteit te bereiken is door bètaverval. Tijdens bètaverval wordt een neutron in de kern omgezet in een proton en een elektron. De emissie van het elektron brengt het aantal positieve ladingen (protonen) en negatieve ladingen (elektronen) in evenwicht, wat leidt tot een stabiele configuratie.
6. Kernreacties: In extreme gevallen kan een atoom met een aanzienlijke onbalans tussen protonen en elektronen kernreacties ondergaan. Deze reacties omvatten de herschikking van protonen en neutronen in de kern om een stabielere configuratie te bereiken.
Het is vermeldenswaard dat het bestaan van een atoom met meer protonen dan elektronen hypothetisch is. In werkelijkheid hebben atomen de neiging een neutrale lading te behouden, waarbij het aantal protonen en elektronen gelijk is. Als een atoom elektronen verliest of krijgt (en een ion wordt), ondergaat het chemische reacties om stabiliteit te bereiken en stabiele verbindingen te vormen.
 Wat zijn de andere subatomaire deeltjes waaruit het magnesiumatoom bestaat, naast protonen en elektronen?
Wat zijn de andere subatomaire deeltjes waaruit het magnesiumatoom bestaat, naast protonen en elektronen?  Snel reagerend, kleurveranderende moleculaire sonde detecteert wanneer een materiaal op het punt staat te falen
Snel reagerend, kleurveranderende moleculaire sonde detecteert wanneer een materiaal op het punt staat te falen Onderzoek levert nieuw ontwerpprincipe op voor watersplitsende katalysatoren
Onderzoek levert nieuw ontwerpprincipe op voor watersplitsende katalysatoren Waarom is het belangrijk om een gelijkwaardig aandeel aan reagentia te handhaven bij de synthese van dibenzalaceton?
Waarom is het belangrijk om een gelijkwaardig aandeel aan reagentia te handhaven bij de synthese van dibenzalaceton?  Zorgt zout dat aan water wordt toegevoegd ervoor dat het water sneller opwarmt dan zonder water, en als beide worden verwarmd, kookt het?
Zorgt zout dat aan water wordt toegevoegd ervoor dat het water sneller opwarmt dan zonder water, en als beide worden verwarmd, kookt het?
 Poten tot nadenken:voelt uw huisdier een complexe emotie?
Poten tot nadenken:voelt uw huisdier een complexe emotie?  Lijst met neolithische gereedschappen voor steen
Lijst met neolithische gereedschappen voor steen  Waarom het koolstofvrij maken van zeevervoer misschien niet van een leien dakje gaat?
Waarom het koolstofvrij maken van zeevervoer misschien niet van een leien dakje gaat? Hoe vulkanen op aarde een venster bieden op de evolutie van het leven en het zonnestelsel
Hoe vulkanen op aarde een venster bieden op de evolutie van het leven en het zonnestelsel Hoe Mushroom Spawn te maken
Hoe Mushroom Spawn te maken
Hoofdlijnen
- Vroegwaarschuwingssysteem voor veranderingen in het milieu:nieuwe dierenlabels met camera's en AI volledige eerste vlucht
- Een evenwicht vinden in de antibioticageneeskunde:kunnen we slechte bacteriën doden en tegelijkertijd de goede behouden?
- Hoe eiwitten gist helpen zich aan te passen aan veranderende omstandigheden
- Soorten collageenvezels
- Trilaminaire structuur van het celmembraan
- Hoe biologen veldwerk veiliger en rechtvaardiger maken
- Hoe lang kunnen virussen op oppervlakken leven?
- Klimaatverandering onthult de ingewikkelde dynamiek van reproductieve barrières bij mariene soorten
- Hoe het verbod op positieve discriminatie selectieve hogescholen en de beroepsbevolking minder divers maakt
- Kristallen kweken om willekeurige getallen te genereren

- Hoe nieuwe materialen de efficiëntie van directe ethanolbrandstofcellen verhogen

- Ze oprollen:organische moleculen synthetiseren met een lange spiraalvormige structuur

- Natuurlijk mineraal hackmaniet vertoont een zeer herhaalbaar kleurveranderingsvermogen

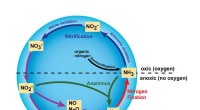
- De fijne kneepjes van de stikstofcyclus onderzoeken
 Smelt plastic flessen voor Molding
Smelt plastic flessen voor Molding Wat beschrijft correct een verschil tussen de mannelijke en vrouwelijke voortplantingssystemen?
Wat beschrijft correct een verschil tussen de mannelijke en vrouwelijke voortplantingssystemen?  Waarom charismatische, geïntroduceerde soorten zo moeilijk te beheren zijn
Waarom charismatische, geïntroduceerde soorten zo moeilijk te beheren zijn  Prototype-telescoop demonstreert levensvatbaarheid van nieuw Schwarzschild-Couder-ontwerp
Prototype-telescoop demonstreert levensvatbaarheid van nieuw Schwarzschild-Couder-ontwerp Facebook werkt samen met onderzoek in New York:openbare aanklager
Facebook werkt samen met onderzoek in New York:openbare aanklager Onderzoek toont aan dat vrouwelijke sekswerkers worden blootgesteld aan extreem veel geweld
Onderzoek toont aan dat vrouwelijke sekswerkers worden blootgesteld aan extreem veel geweld Welke term beschrijft de neiging van een object om weerstand te bieden aan een verandering in beweging?
Welke term beschrijft de neiging van een object om weerstand te bieden aan een verandering in beweging?  Vallen voor energiebronmoleculen in cellen
Vallen voor energiebronmoleculen in cellen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

