
Wetenschap
De verbrandingswarmte heptaan bedraagt 4817 kj per mol. Hoeveel zou er vrijkomen als 250 kg een volledige verbranding ondergaat?
De verbrandingsenthalpie van heptaan bedraagt -4817 kJ/mol. Dit betekent dat wanneer één mol heptaan een volledige verbranding ondergaat, er 4817 kJ aan warmte vrijkomt.
Om de hoeveelheid warmte te berekenen die vrijkomt wanneer 250 kg heptaan een volledige verbranding ondergaat, moeten we eerst de massa heptaan omzetten in mol. De molaire massa van heptaan is 100,2 g/mol, dus 250 kg heptaan is gelijk aan:
$$250\times1000\ g\times\frac{1\ mol}{100,2\ g}=2494,7\ mol$$
Nu kunnen we de verbrandingsenthalpie gebruiken om de hoeveelheid vrijkomende warmte te berekenen:
$$2494,7\ mol\times(-4817\ kJ/mol)=-12030\times10^3\ kJ$$
Wanneer 250 kg heptaan een volledige verbranding ondergaat, komt er dus 12030 MJ aan warmte vrij.
 Vaccin-ingrediënten kunnen zich verbergen in bibliotheken met kleine moleculen
Vaccin-ingrediënten kunnen zich verbergen in bibliotheken met kleine moleculen Met gewone tape, onderzoekers maken chip die de ontwikkeling van medicijnen kan versnellen
Met gewone tape, onderzoekers maken chip die de ontwikkeling van medicijnen kan versnellen Hoeveel atomen zitten er in 169 g calcium?
Hoeveel atomen zitten er in 169 g calcium?  Waar bevinden zich de chemoreceptoren voor de detectie van een laag zuurstofgehalte in het lichaam?
Waar bevinden zich de chemoreceptoren voor de detectie van een laag zuurstofgehalte in het lichaam?  Hoe bloemen een vleugje bling gebruiken om de bijen te verleiden
Hoe bloemen een vleugje bling gebruiken om de bijen te verleiden
 Langlevende tropische bomen spelen een te grote rol bij koolstofopslag
Langlevende tropische bomen spelen een te grote rol bij koolstofopslag NASA's GPM vindt dat Beryls-resten regenen op de Bahama's
NASA's GPM vindt dat Beryls-resten regenen op de Bahama's Australische supermarkt in zakken na plastic backflip
Australische supermarkt in zakken na plastic backflip Lekken tonen de klimaatinspanningen van de groep aan
Lekken tonen de klimaatinspanningen van de groep aan  Wetenschappers luiden alarm over ongekende ophoping van kwik in loopgraven van de Stille Oceaan
Wetenschappers luiden alarm over ongekende ophoping van kwik in loopgraven van de Stille Oceaan
Hoofdlijnen
- Is intelligentie een genetisch kenmerk?
- Nieuw hulpmiddel onthult hoe de verschillende vormen van organismen groeien
- Bonobo's en chimpansees:wat onze naaste familieleden ons over mensen vertellen
- Deskundigen zijn het erover eens:het welzijn van melkvee is slechter dan vleesvee
- Zeesponzen bieden aanwijzingen hoe door de mens gemaakte structuren weerstand kunnen bieden aan knikken
- Insectengedrag bestuderen? Maak van jezelf een ethoscoop
- Zijn religies ontstaan uit ons verkeerde begrip van het menselijk bewustzijn?
- Wat zijn de componenten van nucleotiden?
- Waarom wordt gezegd dat bladeren excretoforen zijn?
- Directe synthese van waterstofperoxide met behulp van TS-1-ondersteunde katalysatoren
- Materiaal om de overgang naar schone waterstofbrandstof te helpen

- Een materiaal ondersteboven keren kan het soms zachter maken

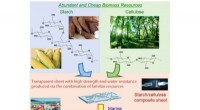
- Onderzoekers maken in water afbreekbaar plastic dat zetmeel en cellulose combineert
- Voordeel:Water—Onderzoekers lossen belangrijke vraag op over titaniumoxide, water interacties

 Mojo Vision pronkt met displaytechnologie voor augmented reality
Mojo Vision pronkt met displaytechnologie voor augmented reality America's Next Top Model:Hoe dragen fans bij aan het verval van hun favoriete tv-programma's?
America's Next Top Model:Hoe dragen fans bij aan het verval van hun favoriete tv-programma's?  Moleculaire schakelaar detecteert metalen in de omgeving
Moleculaire schakelaar detecteert metalen in de omgeving Astronomen zijn op jacht naar Dyson-bollen
Astronomen zijn op jacht naar Dyson-bollen  Zijn ammoniumsulfaat en aluminium hetzelfde?
Zijn ammoniumsulfaat en aluminium hetzelfde?  Onderzoekers bedenken nanodruppels die bijziendheid en verziendheid verbeteren
Onderzoekers bedenken nanodruppels die bijziendheid en verziendheid verbeteren Eigenzinnig zomermoessongedrag beïnvloedt regenval in Oost-Azië
Eigenzinnig zomermoessongedrag beïnvloedt regenval in Oost-Azië Mercuriusovergang waargenomen bij Cerro Tololo Inter-American Observatory
Mercuriusovergang waargenomen bij Cerro Tololo Inter-American Observatory
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

