
Wetenschap
Wetenschappers beschrijven een mogelijk ziekteverwekkend mechanisme bij hypertrofische cardiomyopathie
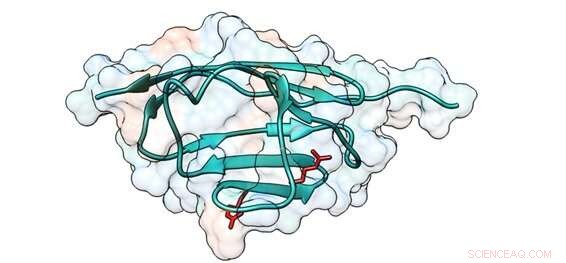
Schema van een cMyBP-C-gebied waarin mutaties aminozuurveranderingen veroorzaken die de mechanische eigenschappen van het eiwit veranderen. De posities van de aangetaste aminozuren zijn in rood weergegeven. Krediet:CNIC
Wetenschappers van het Centro Nacional de Investigaciones Cardiovasculares (CNIC) hebben een potentieel ziekteverwekkend mechanisme beschreven bij hypertrofische cardiomyopathie (HCM), de meest voorkomende erfelijke hartziekte. De studie, gepubliceerd in het tijdschrift ACS Nano , geeft de eerste beschrijving van een verband tussen deze ziekte en mechanische veranderingen aan een onderdeel van de contractiele machinerie van het hart.
De hartspier staat gedurende het hele leven onder constante mechanische stress omdat hij samentrekt om bloed naar het lichaam te pompen. Het laboratorium onder leiding van Dr. Jorge Alegre-Cebollada onderzoekt hoe de mechanische eigenschappen van de harteiwitten het fysiologische gedrag van deze spier bepalen en hoe veranderingen in deze eigenschappen leiden tot het ontstaan van ziekten zoals HCM. Bij deze ziekte, de meest voorkomende erfelijke ziekte die het hart aantast, de linker hartkamer wordt vergroot, en ernstige manifestaties omvatten hartfalen en plotselinge dood.
Wetenschappers weten al meer dan 20 jaar dat HCM wordt veroorzaakt door mutaties in eiwitten met een mechanische functie in het hart. Een van de uitdagingen van cardiovasculaire genetica is om te identificeren welke van de genetische varianten die bij patiënten en hun families worden gevonden, ziekte veroorzaken. Weten of een mutatie al dan niet ziekteverwekkend is, is belangrijk omdat deze informatie bepalend is voor de klinische follow-up van familieleden en, mogelijk, hun behandeling.
De nieuwe studie, gecoördineerd door Dr. Jorge Alegre-Cebollada, geanalyseerd cardiaal myosine-bindend eiwit C (cMyBP-C).
Eerste auteur Carmen Suay-Corredera legde uit dat cMyBP-C, die de hartcontractie reguleert, is het meest gemuteerde eiwit bij HCM-patiënten. "Een groot deel van de mutaties in het cMyBP-C-gen veroorzaakt aminozuurveranderingen in het eiwit; de mechanismen waarmee deze mutaties HCM veroorzaken, zijn niet precies bekend."
Dr. Alegre-Cebollada's groep, in nauwe samenwerking met klinische en moleculaire onderzoekers in Europa en de VS, het opzetten van een database van cMyBP-C-varianten met een duidelijke link naar HCM om de moleculaire defecten die ten grondslag liggen aan de ziekte te definiëren.
Met behulp van bio-informatica en experimentele benaderingen, het onderzoeksteam ontdekte dat ongeveer de helft van deze mutaties de integriteit van cMyBP-C messenger RNA (mRNA) of eiwit aantast. Deze resultaten zijn al geaccepteerd voor publicatie in de Tijdschrift voor biologische chemie en zijn het onderwerp geweest van een commentaarartikel in het toonaangevende tijdschrift voor medische genetica Genetica in de geneeskunde .
Hoewel veranderingen in de mRNA- of eiwitintegriteit de pathogeniteit van de helft van de in de eerdere studie geanalyseerde mutaties zouden kunnen verklaren, Suay-Carredera wees erop dat de andere helft via deze route geen ziekte veroorzaakt.
“Het zijn juist deze varianten, die HCM veroorzaken via onbekende mechanismen, die we in de nieuwe studie hebben geanalyseerd, " verklaarde Dr. Alegre-Cebollada, die de groep Molecular Mechanics of the Cardiovascular System bij het CNIC leidt.
Met behulp van geavanceerde biofysische technieken gebaseerd op atoomkrachtmicroscopie, het team toonde aan dat sommige van de ziekteverwekkende mutaties in cMyBP-C defecten veroorzaken in de mechanische eigenschappen van het eiwit die de contractiele functie van cardiomyocyten bij HCM-patiënten kunnen veranderen.
"We onderzoeken nu de ziekteverwekkende mechanismen van die varianten die niet zijn gekoppeld aan enige relevante wijziging in eerdere studies, " zei Dr. Alegre-Cebollada. Voor dit project, de wetenschappers werken met een reeks experimentele systemen, van moleculaire systemen tot diermodellen van HCM.
Het identificeren van de moleculaire mechanismen die ten grondslag liggen aan HCM is essentieel om te bepalen welke cMyBP-C-mutaties de ziekte veroorzaken. Deze kennis is dus ook cruciaal voor de klinische opvolging en eventuele behandeling van patiënten en hun families, zeggen de auteurs.
 Kalium geeft op perovskiet gebaseerde zonnecellen een efficiëntieboost
Kalium geeft op perovskiet gebaseerde zonnecellen een efficiëntieboost 2-D moleculaire kristallen die de elektronische eigenschappen van organische halfgeleiders moduleren
2-D moleculaire kristallen die de elektronische eigenschappen van organische halfgeleiders moduleren Wetenschappers creëren nieuw Y-vormig synthetisch consortium voor efficiënte bioproductie
Wetenschappers creëren nieuw Y-vormig synthetisch consortium voor efficiënte bioproductie Wetenschappers vinden nieuwe methode om elektronische eigenschappen van nanokristallen te controleren
Wetenschappers vinden nieuwe methode om elektronische eigenschappen van nanokristallen te controleren Hoe methaangas te detecteren
Hoe methaangas te detecteren
 Filipijnse hoofdstad opgeschrikt door aardbeving
Filipijnse hoofdstad opgeschrikt door aardbeving De effecten van een cycloon
De effecten van een cycloon De meeste van de laatste 11, 000 jaar koeler dan het afgelopen decennium in Noord-Amerika, Europa
De meeste van de laatste 11, 000 jaar koeler dan het afgelopen decennium in Noord-Amerika, Europa Spoorgassen uit de oceaan zijn bron van deeltjes die de klimaatverandering op Antarctica versnellen
Spoorgassen uit de oceaan zijn bron van deeltjes die de klimaatverandering op Antarctica versnellen UTSA maakt webgebaseerd open source-dashboard van North Pole
UTSA maakt webgebaseerd open source-dashboard van North Pole
Hoofdlijnen
- Hoe celstructuren te identificeren
- Genontdekking kan wereldwijde tarwe-epidemie stoppen
- Vroege mensen gepaard met ingeteelde neanderthalers - tegen een prijs
- Aanvallen van rupsen zorgen ervoor dat bladluizen planten kunnen besluipen
- Wat is een adaptief voordeel voor het beperken van DNA in een kern?
- Routes uit isolatie voor Yellowstone grizzlyberen
- Projectideeën om het menselijke spijsverteringsstelsel te laten zien op de middelbare school voor studenten
- Your Brain On: Exam Stress
- Hoe een zevende-graadsmodel van een dierencel te bouwen
- Antiferromagnetische fluoride nanokristallen
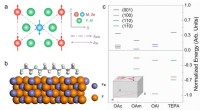
- Onderzoekers gebruiken silicium nanodeeltjes om de efficiëntie van zonnecellen te verbeteren

- Groovy sleutel tot nanobuisjes in 2-D

- Natuurkundigen leggen eerste beelden vast van atoomspin
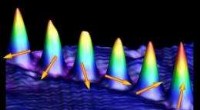
- Natuurkundigen meten voor het eerst van der Waals-krachten van individuele atomen

 Nanodeeltjes verhogen de intensiteit van de gloed van Quantum Dots
Nanodeeltjes verhogen de intensiteit van de gloed van Quantum Dots Onderzoekers deconstrueren oud Joods perkament met behulp van meerdere beeldvormingstechnieken
Onderzoekers deconstrueren oud Joods perkament met behulp van meerdere beeldvormingstechnieken Een slimme auto die hersensignalen kan lezen
Een slimme auto die hersensignalen kan lezen Bereken paardekracht & RPM
Bereken paardekracht & RPM  VS worstelt om bij te blijven terwijl de hennepindustrie groeit
VS worstelt om bij te blijven terwijl de hennepindustrie groeit Onderzoekers ontwikkelen EV-batterijmaterialen met hoge capaciteit die het rijbereik verdubbelen
Onderzoekers ontwikkelen EV-batterijmaterialen met hoge capaciteit die het rijbereik verdubbelen Hoe molaire oplosbaarheid te berekenen uit KSP?
Hoe molaire oplosbaarheid te berekenen uit KSP?  Onderzoekers ontdekken nieuw materiaal:zwart zilver
Onderzoekers ontdekken nieuw materiaal:zwart zilver
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

