
Wetenschap
De atoomtheorie van John Dalton:sleutelprincipes en impact
1. Alle materie bestaat uit kleine, ondeelbare deeltjes die atomen worden genoemd. Dit was een radicale afwijking van het heersende idee dat materie continu is. Dalton stelde dat alle materie, hoe complex ook, bestaat uit deze fundamentele bouwstenen.
2. Atomen van een bepaald element zijn identiek in grootte, massa en andere eigenschappen. Dit betekende dat alle atomen van een specifiek element, zoals zuurstof of koolstof, in wezen hetzelfde waren.
3. Atomen van verschillende elementen hebben verschillende eigenschappen. Dit verklaarde waarom verschillende elementen unieke kenmerken hebben. Goud verschilt bijvoorbeeld van zilver omdat goudatomen andere eigenschappen hebben dan zilveratomen.
4. Atomen kunnen niet worden gecreëerd of vernietigd tijdens chemische reacties. Dit is de wet van behoud van massa, die stelt dat materie noch kan ontstaan, noch vernietigd kan worden door chemische reacties. De theorie van Dalton verklaarde dit door te stellen dat atomen zichzelf eenvoudigweg herschikken tijdens chemische reacties.
5. Chemische verbindingen worden gevormd wanneer atomen van verschillende elementen samenkomen in vaste gehele getalsverhoudingen. Dit verklaarde de consistente samenstelling van verbindingen. Water bevat bijvoorbeeld altijd twee waterstofatomen voor elk zuurstofatoom.
Daltons atoomtheorie was weliswaar niet geheel accuraat (we weten nu dat atomen in kleinere deeltjes kunnen worden verdeeld), maar was een opmerkelijke prestatie. Het bood een raamwerk voor het begrijpen van de aard van de materie en legde de basis voor de ontwikkeling van de moderne chemie.
Hoofdlijnen
- Wilde genen bij gedomesticeerde soorten:hoe we onze gewassen een boost kunnen geven met behulp van hun verre verwanten
- De verschillen tussen Catecholamines en Cortisol
- Kun je onderscheid maken tussen een prokaryoctische cel en eukaryoctische cel?
- Waarom zijn neuronen en spiercellen rijk aan mitochondriën?
- Wat zijn de gelijkenissen tussen planten- en dierlijke cellen?
- Wat is de functie van Golgi -lichaam een plantencel?
- Welke vormen wanneer bestuiving plaatsvindt, zijn het zaden?
- Wat betekent het dat een populatie in genetisch evenwicht is?
- Aten Neanderthalers hun groenten? Studie levert het eerste directe bewijs van planten in het Neanderthaler-dieet
- Effectieve temperaturen verbinden evenwichts- en niet-evenwichtssystemen

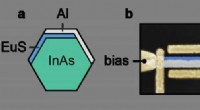
- Samenwerking levert veelbelovend materiaal op voor quantum computing
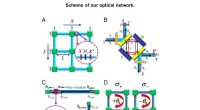
- Een nieuw concept voor een unidirectionele golfgeleider
- Opgewaardeerde laserfaciliteit maakt de weg vrij voor deeltjesversnellers van de volgende generatie

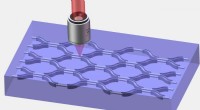
- Golfgeleider met laag buigverlies opent de weg naar inkrimping van 3D fotonische geïntegreerde schakelingen
 Wat is een betere bron van energiebron conventionele en niet -bronnen energie?
Wat is een betere bron van energiebron conventionele en niet -bronnen energie?  Narco-drones zijn de nieuwste vorm van drugshandel. Onze wetten zijn nog niet klaar om ze te bestrijden
Narco-drones zijn de nieuwste vorm van drugshandel. Onze wetten zijn nog niet klaar om ze te bestrijden Waarom zouden we energie besparen?
Waarom zouden we energie besparen?  Waarom versnellen objecten met minder massa met een hoger tempo?
Waarom versnellen objecten met minder massa met een hoger tempo?  Wat zijn enkele nadelen van biologische energie?
Wat zijn enkele nadelen van biologische energie?  Factoren van ecologische successie
Factoren van ecologische successie Hoe is het momentum van een object gerelateerd aan de stopafstand?
Hoe is het momentum van een object gerelateerd aan de stopafstand?  Onderzoekers werken meetverhoudingen bij voor fusie-experimenten met traagheidsopsluiting
Onderzoekers werken meetverhoudingen bij voor fusie-experimenten met traagheidsopsluiting
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


