
Wetenschap
Hoe trekt de afstand tussen deeltjes aan?
* Elektrostatische krachten: Deze krachten komen voort uit de aantrekkingskracht tussen tegengestelde ladingen. Positief geladen deeltjes trekken negatief geladen deeltjes aan. Dit is een fundamentele kracht die een belangrijke rol speelt bij het samen houden van atomen in moleculen en moleculen in vaste stoffen en vloeistoffen.
* zwaartekrachten: Hoewel veel zwakker dan elektrostatische krachten, is de zwaartekracht altijd aantrekkelijk. Het werkt tussen twee objecten met massa, inclusief deeltjes. De zwaartekracht wordt echter alleen significant op grotere schalen zoals planeten of sterren.
* van der Waals krachten: Dit zijn zwakkere krachten die voortkomen uit tijdelijke schommelingen in elektronenverdeling rond atomen. Ze zijn verantwoordelijk voor attracties tussen niet -polaire moleculen en spelen een rol bij het bij elkaar houden van sommige vloeistoffen en vaste stoffen.
Hoe afstand de aantrekkingskracht beïnvloedt:
* Elektrostatische krachten: De sterkte van elektrostatische aantrekkingskracht neemt snel af naarmate de afstand tussen deeltjes toeneemt. Dit volgt op een omgekeerde vierkante wet, wat betekent dat als u de afstand verdubbelt, de aantrekkingskracht vier keer zwakker wordt.
* zwaartekrachten: Evenzo neemt de aantrekkingskracht van de zwaartekracht ook af met afstand, na een omgekeerde vierkante wet.
* van der Waals krachten: Deze krachten zijn nog gevoeliger voor afstand. Het zijn zeer korte-afstandskrachten, wat betekent dat ze na een bepaalde afstand te verwaarlozen worden.
Samenvattend:
Hoewel afstand niet direct deeltjes aantrekt, speelt het een cruciale rol bij het bepalen van de sterkte van aantrekkelijke krachten tussen hen. Hoe verder uit elkaar deeltjes zijn, hoe zwakker de aantrekkingskracht ertussen, ongeacht het type kracht.
 Wat is de moleculaire formule voor 2-butyne?
Wat is de moleculaire formule voor 2-butyne?  Zullen cesium en zwavel een binding vormen?
Zullen cesium en zwavel een binding vormen?  Wat is het verschil tussen ijzeratoom en een natriumatoom?
Wat is het verschil tussen ijzeratoom en een natriumatoom?  Wat is de algehele lading van een heliumatoom met 2 protonen neutronen en elektronen?
Wat is de algehele lading van een heliumatoom met 2 protonen neutronen en elektronen?  Wanneer u vaste suiker in water oplost, zal deze nieuwe oplossing zoet smaken en door een chemische verandering gaan?
Wanneer u vaste suiker in water oplost, zal deze nieuwe oplossing zoet smaken en door een chemische verandering gaan?
 Hoe beïnvloedt het klimaat de hoogte of hoogte?
Hoe beïnvloedt het klimaat de hoogte of hoogte?  Cyprus-studie toont grote daling van verontreinigende stoffen tijdens lockdown
Cyprus-studie toont grote daling van verontreinigende stoffen tijdens lockdown Evacuaties besteld terwijl Florida zich schrap zet voor orkaan Michael
Evacuaties besteld terwijl Florida zich schrap zet voor orkaan Michael Methoden voor verwijdering van huishoudelijk afval
Methoden voor verwijdering van huishoudelijk afval  Waarom hebben grassen het moeilijk om in het bos te wonen?
Waarom hebben grassen het moeilijk om in het bos te wonen?
Hoofdlijnen
- Het perengenoom kraken:hoe studenten hielpen een nieuw hulpmiddel voor de industrie te ontsluiten
- Een garnalenverhaal - winnaars en verliezers in klimaatverandering
- Hoe worden enzym meestal genoemd?
- Blauw licht is de belangrijkste factor die de fotodegradatie van bladafval beïnvloedt
- Bestaat er een geloofwaardige wetenschappelijke theorie die evolutie tegenspreekt?
- Welk orgaan verwijdert water en absorbeert het terug in je lichaam?
- Uit herbebossingsonderzoek blijkt dat slechts enkele boomsoorten een eeuw van snelle klimaatverandering kunnen overleven
- Is het een neushoorn? Nieuwe DNA-test identificeert hoorns sneller om stropers te vangen
- Uitleggen hoe de hersenen gezichten herkennen
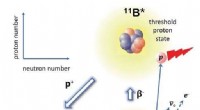
- Handige locatie van een bijna-drempel proton-emitterende resonantie in boor-11
- Foutgevoelige kwantumbits kunnen zichzelf corrigeren, natuurkundigen laten zien

- Natuurkundigen hebben licht door het vlak van 's werelds dunste halfgeleiderkristal gelaten

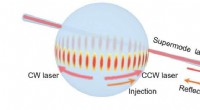
- Gestimuleerde verstrooiing in supermode microcavities:single- of dual-mode laseren?
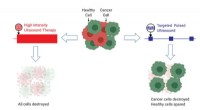
- Echografie beschadigt selectief kankercellen wanneer ze worden afgestemd om frequenties te corrigeren
 Wie heeft de mogelijkheid om lichte energie om te zetten in chemische energie?
Wie heeft de mogelijkheid om lichte energie om te zetten in chemische energie?  Californische wetgevers stemmen om de terugdraaiing van het milieu van Trump te blokkeren, Newsom trotseren
Californische wetgevers stemmen om de terugdraaiing van het milieu van Trump te blokkeren, Newsom trotseren Waar worden vulkanen met ijzerrijke rotsen gevonden?
Waar worden vulkanen met ijzerrijke rotsen gevonden?  Ford viert eeuw productie in legendarische fabriek in Rouge
Ford viert eeuw productie in legendarische fabriek in Rouge Wat gebeurt er als een vogel een vliegtuig raakt?
Wat gebeurt er als een vogel een vliegtuig raakt?  Welke basisvorm van energie is aanwezig in een vibrerende trommel?
Welke basisvorm van energie is aanwezig in een vibrerende trommel?  Welke organismen leven in modderzand en rots op de oceaanbodem?
Welke organismen leven in modderzand en rots op de oceaanbodem?  Onderzoeker past nieuw materiaalonderzoek toe om ontzilting goedkoper en efficiënter te maken
Onderzoeker past nieuw materiaalonderzoek toe om ontzilting goedkoper en efficiënter te maken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

