
Wetenschap
Wat is het maximale aantal ongepaarde elektronen in S -subshell en D P F Subshell?
* s subshell: De S -subshell kan maximaal 2 elektronen bevatten. Het maximale aantal ongepaard Elektronen in een S -subshell is 1 . Dit komt omdat de twee elektronen in een S -subshell tegengestelde spins hebben.
* P Subshell: De P -subshell kan maximaal 6 elektronen bevatten. Het maximale aantal ongepaard Elektronen in een P -subshell is 3 . Dit komt omdat de drie orbitalen binnen de P -subshell elk één elektron vasthouden met dezelfde draai voordat je het koppelt.
* d subshell: De D -subshell kan maximaal 10 elektronen bevatten. Het maximale aantal ongepaard Elektronen in een D -subshell is 5 . Nogmaals, elk van de vijf D -orbitalen kan één elektron met dezelfde draai vasthouden voordat ze worden gekoppeld.
* f Subshell: De F -subshell kan maximaal 14 elektronen bevatten. Het maximale aantal ongepaard Elektronen in een F -subshell is 7 . Elk van de zeven F -orbitalen kan één elektron met dezelfde draai vasthouden voordat ze worden gekoppeld.
Key Principle: Elektronen zullen elk orbitaal individueel binnen een subshell bezetten voordat ze in hetzelfde orbitaal worden gekoppeld. Dit komt door de heerschappij van Hund, die de afstoting van elektronen-elektronen minimaliseert.
 Wat is de belangrijke gecodeerde informatie in een organische verbinding?
Wat is de belangrijke gecodeerde informatie in een organische verbinding?  Stoffen groeien uit wanneer verhit omdat de moleculen?
Stoffen groeien uit wanneer verhit omdat de moleculen?  Doorbraak voor wetshandhavers om hennep en gecontroleerde marihuana snel te onderscheiden
Doorbraak voor wetshandhavers om hennep en gecontroleerde marihuana snel te onderscheiden Wat is chromische sulfideformule?
Wat is chromische sulfideformule?  Wat zijn de effecten van chloorgas op elektronische componenten?
Wat zijn de effecten van chloorgas op elektronische componenten?
Hoofdlijnen
- Hoe noem je een groep organen die samenwerken om een belangrijke functie uit te voeren?
- Welke functie vervullen spillen tijdens mitose?
- Bevat ATP de suikerglucose?
- Wat zijn fossielen en wat vertellen ze ons over het evolutieproces?
- Welk enzym breekt disacchariden af?
- Genetici lossen een veertig jaar oud dilemma op om te verklaren waarom dubbele genen in het genoom achterblijven
- Race om Indonesische krokodil te redden die is getroffen door een bandenketting
- Wat zijn delen van het Calamansi -zaadje?
- Waar is de kant van het DNA -laatste molecuul op?
- Ogen op VENUS:ORNL levert unieke Amerikaanse neutronenbeeldvormingscapaciteit voor wetenschappelijke ontdekking

- Wet van roetlichtabsorptie:huidige klimaatmodellen onderschatten opwarming door zwarte koolstofaërosol

- Onderzoekers realiseren kwantumteleportatie op mechanische beweging van siliciumstralen

- Hoe het opwarmen van een kwantumsysteem kan worden gebruikt als een universele sonde voor exotische toestanden van materie

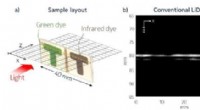
- Onderzoekers demonstreren chemisch gevoelige LiDAR-methode
 Welk bewegingspatroon wordt geïdentificeerd met de wetsinertie?
Welk bewegingspatroon wordt geïdentificeerd met de wetsinertie?  Hoe snel reist geluid door een solide in MPH?
Hoe snel reist geluid door een solide in MPH?  Onderzoekers observeren de golf-deeltjesdualiteit van twee fotonen
Onderzoekers observeren de golf-deeltjesdualiteit van twee fotonen  Simpele verwering en erosie-experimenten voor de derde graad
Simpele verwering en erosie-experimenten voor de derde graad  Facebook gaat regels voor politieke advertenties aanscherpen voor verkiezingen van 2019
Facebook gaat regels voor politieke advertenties aanscherpen voor verkiezingen van 2019 Wat is ruimteladingpolarisatie?
Wat is ruimteladingpolarisatie?  Hoe is de zonne -energie en wind anders?
Hoe is de zonne -energie en wind anders?  Hoe schrijf je hco2?
Hoe schrijf je hco2?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

