
Wetenschap
Hoe was de hoofdtheorie op het moment van experiment hoe Atom eruit zag?
Dit model was gebaseerd op de volgende ontdekkingen:
* Ontdekking van het elektron: Thomson's eigen werk had het bestaan aangetoond van negatief geladen deeltjes (elektronen) in atomen.
* Atom's Neutrality: Atomen zijn elektrisch neutraal, wat de aanwezigheid van zowel positieve als negatieve ladingen impliceert.
Het pruimpuddingmodel had echter enkele tekortkomingen:
* Gebrek aan een gedefinieerde kern: Het verklaarde niet waarom atomen zo stabiel waren, omdat de positieve lading uniform werd verdeeld over het atoom.
* verstrooiing van alfa -deeltjes: Het experiment van Rutherford toonde aan dat sommige alfa -deeltjes onder grote hoeken werden afgebogen, wat het pruimpuddingmodel niet kon verklaren.
Het experiment van Rutherford weerlegde uiteindelijk het pruimpuddingmodel en leidde tot de ontwikkeling van het nucleaire model van het atoom . Dit model stelde een dichte, positief geladen kern voor in het midden van het atoom, met elektronen die eromheen draaien.
 Wat is de elektronencapaciteit van de tweede schil?
Wat is de elektronencapaciteit van de tweede schil?  Onderzoekers ontdekken een milieuvriendelijk fungicidenalternatief
Onderzoekers ontdekken een milieuvriendelijk fungicidenalternatief  Waterstofonderzoek voedt nieuwe zonne-ideeën voor groene energie
Waterstofonderzoek voedt nieuwe zonne-ideeën voor groene energie Wat gebeurt er met koelmiddel in de condensor?
Wat gebeurt er met koelmiddel in de condensor?  Wat is de chemische naam van droog ijs. Waarom is het geroepen, is ijs hetzelfde als gewoon ijs?
Wat is de chemische naam van droog ijs. Waarom is het geroepen, is ijs hetzelfde als gewoon ijs?
 Onderzoekers ontwikkelen radars in de lucht om de kenmerken van Amerikaanse snowpacks voor watermodellen te meten
Onderzoekers ontwikkelen radars in de lucht om de kenmerken van Amerikaanse snowpacks voor watermodellen te meten Hoe identificeer ik een ecosysteem?
Hoe identificeer ik een ecosysteem?  Copepods:de onbezongen helden van de oceaan
Copepods:de onbezongen helden van de oceaan Bestudeer gebieden met hoge concentraties in de Delaware Bay
Bestudeer gebieden met hoge concentraties in de Delaware Bay Wat zou je kunnen vinden in een Maya -regenwoud?
Wat zou je kunnen vinden in een Maya -regenwoud?
Hoofdlijnen
- Onderzoekers ontdekken een parallel universum in de tomatengenetica
- Vergelijk de algemene rol van mitose en meiose bij plantendier?
- Proteomische analyse laat zien hoe fosfiet bijdraagt aan de strijd tegen chemisch resistente afsterving
- Klimaatverandering is de meest prominente bedreiging voor bestuivers, zo blijkt uit onderzoek
- Welke van de volgende moleculen verbindt zich om zetmeel te vormen?
- Waarom Bacillus cereus meer hittebestendig dan Aspergillus niger?
- Hoe denken wetenschappers dat het eerste meercellige organisme is ontstaan?
- Wat is de Chromatins-functie?
- Wat wordt gebruikt om aan te tonen dat het DNA -molecuul een helix?
- Herscheppen van supernovareactie levert nieuwe inzichten op voor fusie-energie

- Onderzoek opent deur naar kleinere, goedkoper, meer flexibele communicatietechnologie

- Temperatuurontwikkeling van onzuiverheden in een kwantumgas
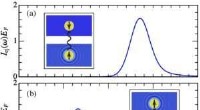
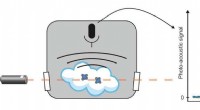
- Een wereldrecord in het detecteren van extreem lage niveaus van gasonzuiverheden
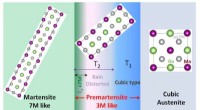
- Robuuste Bain-vervorming in de premartensietfase van een platina-gesubstitueerd Ni2MnGa
 Gecontroleerde synthese van kristalvlokken baant pad voor geavanceerde toekomstige elektronica
Gecontroleerde synthese van kristalvlokken baant pad voor geavanceerde toekomstige elektronica Worden fotonen op enigerlei wijze beïnvloed door de zwaartekracht?
Worden fotonen op enigerlei wijze beïnvloed door de zwaartekracht?  HP wijst overnamebod van Xerox af
HP wijst overnamebod van Xerox af Nanomotoren worden aangestuurd, Voor de eerste keer, in levende cellen (met video)
Nanomotoren worden aangestuurd, Voor de eerste keer, in levende cellen (met video) Verboden kruiden? De effecten van cannabis waren 250 jaar geleden een controversieel onderwerp
Verboden kruiden? De effecten van cannabis waren 250 jaar geleden een controversieel onderwerp  Biohybride microrobots kunnen micro- en nanoplastics uit aquatische omgevingen verwijderen
Biohybride microrobots kunnen micro- en nanoplastics uit aquatische omgevingen verwijderen  Trickle-down is de oplossing (voor het probleem van planetaire kernvorming)
Trickle-down is de oplossing (voor het probleem van planetaire kernvorming) wat zijn ionische bindingen?
wat zijn ionische bindingen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

