
Wetenschap
De wetenschap achter de roestverspreiding op ijzer en staal
Door Lauren Vork Bijgewerkt op 24 maart 2022
Wat roest is
Wat roest is
Om te begrijpen hoe roest werkt en zich verspreidt, moet je eerst begrijpen wat roest is. 'Roest' is de algemene naam voor wat wetenschappelijk bekend staat als ijzeroxide, een vorm van corrosie die optreedt wanneer ijzer (of een van zijn legeringen, zoals staal) reageert met zuurstof en er water (of zwaar luchtvochtigheid) aanwezig is.
Andere metalen ondergaan ook oxidatieprocessen, maar ze doen dit op een andere manier en het resultaat wordt doorgaans niet als roest beschouwd. Kopercorrosie is groen (en verklaart de kleur van het Vrijheidsbeeld), terwijl aluminiumcorrosie zich extreem langzaam verspreidt.
Het moleculaire proces van verspreiding
Het moleculaire proces van verspreiding
Het proces van metaalcorrosie is een elektrochemisch proces. Het gebeurt op moleculair niveau wanneer elektronen overgaan van ijzermoleculen naar de omringende zuurstofmoleculen, waardoor de samenstelling van het ijzer verandert en het in roest verandert. Dit gebeurt voortdurend met ijzer. In feite is het onmogelijk om een stuk ijzer te vinden zonder dat er tenminste wat oxide in aanwezig is. De roestsnelheid is echter meestal gering en langzaam, maar wordt versneld door water, vooral als het water een hoge concentratie elektrolyten bevat (stoffen in het water die elektronen helpen bewegen). Daarom zorgt de aanwezigheid van zout ervoor dat roest zich sneller verspreidt.
Verspreiding
Verspreiding
Roest verspreidt zich niet door contact zoals een biologische infectie. In plaats daarvan vindt het proces van ijzeroxidatie onafhankelijk plaats, afhankelijk van de omstandigheden rondom een bepaald stuk metaal. Dit betekent dat als een deel van het stuk wordt blootgesteld aan water, zuurstof en elektrolyten, maar de roest van het stuk schoon en droog wordt gehouden, het beschermde metaal niet in dezelfde mate zal rusten als het natte metaal.
IJzerlegeringen hebben verschillende corrosiesnelheden, afhankelijk van hun samenstelling.
Hoe preventie werkt
Hoe preventie werkt
Staal wordt gewoonlijk beschermd tegen roesten door middel van een proces dat bekend staat als galvanisatie. Bij dit proces wordt het staal ondergedompeld in een zinklaag, die het staal beschermt door te reageren met watermoleculen. Als de zinklaag op een stuk gegalvaniseerd staal wordt weggekrast of geschraapt, is het blootgestelde gebied kwetsbaar voor roest.
 Loofbomen:kenmerken en waarom ze hun bladeren verliezen
Loofbomen:kenmerken en waarom ze hun bladeren verliezen  Welke details creëren een sfeer van gevaar?
Welke details creëren een sfeer van gevaar?  Waar ter wereld is schade aan het landschap dat wordt veroorzaakt door toerisme?
Waar ter wereld is schade aan het landschap dat wordt veroorzaakt door toerisme?  Onderzoekers wenden zich tot oesters als schildwachten voor het opsporen van vervuiling
Onderzoekers wenden zich tot oesters als schildwachten voor het opsporen van vervuiling Hoe een plantenapp de gevolgen van klimaatverandering helpt identificeren
Hoe een plantenapp de gevolgen van klimaatverandering helpt identificeren
Hoofdlijnen
- Welke geërfde eigenschappen hebben planten?
- Welk deel van een dierencel laat voedselwater en zuurstof doorgaan?
- Wie was de eerste persoon die ontdekte dat alle planten uit cellen bestaan?
- Iets in de invieuring dat het gedrag van een organisme beïnvloedt, is een wat?
- Wat gebeurt er met de structuren in kern elke fase profase plus?
- Wat is de wetenschappelijke naam van Eggwhite?
- Wat is het tegenovergestelde van de erfelijke eigenschap?
- Wat wordt gevormd na ovulatie uit de lege follikel vanwege LH -invloed?
- Wat wij de structuur die een embryo verbindt met orgel voedt embryo?
- De essentiële rol van water in fotosynthese:het leven op aarde voeden

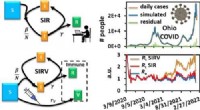
- Chemielabstudenten voorspellen verspreiding van COVID-19 met kinetische modellen
- Commercieel relevante op bismut gebaseerde dunnefilmverwerking

- Kunnen we plastic tassen recyclen tot stoffen van de toekomst?

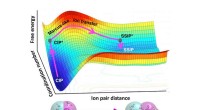
- Elegante theorie laat zien hoe water helpt bij het scheiden van ionen die betrokken zijn bij materiaalsynthese en productie
 NASA vindt post-tropische depressie Cristobal die de Grote Meren doorweekt
NASA vindt post-tropische depressie Cristobal die de Grote Meren doorweekt Waar vindt u geodes
Waar vindt u geodes Welke phyla van protisten wordt gekenmerkt door dieren die zwemmen met behulp van flagella?
Welke phyla van protisten wordt gekenmerkt door dieren die zwemmen met behulp van flagella?  Zonne- en sterrendagen begrijpen:hoe de rotatie van de aarde en de baan de tijd vormen
Zonne- en sterrendagen begrijpen:hoe de rotatie van de aarde en de baan de tijd vormen  Antenne maakt geavanceerde testen van satellietcommunicatie mogelijk
Antenne maakt geavanceerde testen van satellietcommunicatie mogelijk Wie ontdekte Oxygen First Preisty of Cavoiser?
Wie ontdekte Oxygen First Preisty of Cavoiser?  Wat is de relatie tussen vrije energie en stabiliteitswerkcapaciteit?
Wat is de relatie tussen vrije energie en stabiliteitswerkcapaciteit?  Dankzij de techniek voor het bewerken van genen kunnen zijderupsen spinnenzijde produceren
Dankzij de techniek voor het bewerken van genen kunnen zijderupsen spinnenzijde produceren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

